Изменения экг в острый период инфаркта миокарда. Виды инфаркта миокарда по локализации на экг. Варианты инфаркта на ЭКГ
На чтение 6 мин. Просмотров 773
(ИМ) — патология системы сердца и сосудов, которую пациенты часто путают со стенокардией. Однако в отличие от последнего состояния, ИМ при несвоевременном оказании квалифицированной помощи приводит к тяжелым последствиям: инвалидизации пациента или даже летальному исходу.
ЭКГ при инфаркте миокарда — методика, позволяющая обнаружить признаки угрожающего жизни состояния еще на начальных стадиях.
Так же как и сам инфаркт, изменения на ЭКГ при данной нозологии можно классифицировать в зависимости от стадии ишемии, размера пораженного очага и его локализации.
В зависимости от стадии
Кардиограмма при инфаркте позволяет выявить изменения строгого временного характера. Электрокардиографическая кривая различается в зависимости от стадии заболевания и проявления степени ишемии и некроза.
Стадии инфаркта включают в себя следующие этапы.
Как часто Вы сдаете анализ крови?
Poll Options are limited because JavaScript is disabled in your browser.
Только по назначению лечащего врача 30%, 661 голос
Один раз в год и считаю этого достаточно 17%, 371 голос
Как минимум два раза в год 15%, 322 голоса
Чаще чем два раза в год но меньше шести раз 11%, 248 голосов
Я слежу за своим здоровьем и сдаю раз в месяц 7%, 151 голос
Боюсь эту процедуру и стараюсь не сдавать 4%, 96 голосов
21.10.2019
Первые часы сопровождаются различной степенью повреждения сердечной мышцы вследствие ишемии — острейшая фаза. Для нее характерно:
- кривая монофазного типа, возникшая из-за слияния сегмента ST c высоким зубцом T, — это главный признак ЭКГ;
- наличие или отсутствие зубца Q, вызванного некротическими изменениями в ткани миокарда;
- исчезновение зубца R (наблюдается в тех случаях, когда появляется глубокий Q на кардиограмме).
При острой стадии, продолжительность которой колеблется от 2 до 10 суток, наблюдается:
- формирование отрицательного Т или полное его отсутствие;
- большое возвышение сегмента ST по отношению к изолинии, которая располагается над областью нарушения кровообращения;
- Q становится глубже вплоть до появления QT-комплекса.
В подострой (30-60 сутки) наблюдаются следующие показатели кардиограммы:
- зубец T ниже изолинии, амплитуда его увеличивается за счет расширения обескровленной зоны. Нормализуется зубец только во второй половине подострой стадии;
- снижение ST сегмента вплоть до окончания подострой стадии;
- для первых 3 стадий характерны важные особенности электрокардиографической кривой: подъем ST в отведениях, которые соответствуют зоне повреждения и, наоборот, снижение в противоположных ишемическим изменениям участках сердечной мышцы.

Для рубцовой стадии (длительность составляет 7-90 дней) характерно:
- достижение зубцом T изолинии либо положительное его расположение;
- если при острой стадии появляется патологический Q, в рубцовой он сохраняется;
- R становится выше.
В зависимости от размера очага
Электрокардиограмма также может различаться в зависимости от того, насколько обширную зону волокон сердечной мышцы затронуло нарушение кровотока в сосудах.
При ишемии в крупных сосудистых стволах поражение носит обширный характер, тогда как мини-инфаркты сопровождаются нарушением кровоснабжения концевыми артериальными ветвями.
Определить инфаркт на ЭКГ можно по признакам, которые зависят от его размера:
- Крупноочаговый трансмуральный (при данном типе патологии затронута вся толща кардиальной стенки):
- отсутствует зубец R;
- Q расширенный и глубокий;
- слияние ST с зубцом T над зоной ишемии
- Т ниже изолинии в подострой стадии.
- Крупноочаговый субэпикардиальный (локализация инфаркта в зоне рядом с эпикардом):
- наличие уменьшенного зубца R;
- глубокий и широкий зубец Q, который переходит в высокий ST;
- зубец T отрицательный в подострой стадии.
- Мелкоочаговый интрамуральный инфаркт (характерна локализация во внутренних слоях кардиальной мышцы).
- не затронуты зубцы R и Q;
- изменения в сегменте ST отсутствуют;
- на протяжении 14 дней сохраняется T, расположенный ниже изолинии.
- Мелкоочаговый субэндокардиальный:
- патология R и Q не выявляется;
- ST на 0,02 mV и более опускается ниже изолинии;
- зубец T сглажен.
Важная информация: Какие препараты принимать после инфаркта миокарда

При разном расположении инфаркта
Локализация зоны ишемии — еще один фактор, который влияет на ЭКГ признаки инфаркта миокарда.
Расшифровка инфаркта миокарда на ЭКГ осуществляется в 12 отведениях, каждое из которых отвечает за соответствующий участок сердечной мышцы.
Стандартные отведения:
- І — отображает информацию об изменениях, локализованных в передней и боковой части левого желудочка;
- ІІІ — позволяет оценить состояние задней части диафрагмальной поверхности сердца;
- ІІ отведение используется с целью подтверждения данных, полученных при оценке І или ІІІ отведения.
Усиленные отведения:
- aVL (усиленное от левой руки) — позволяет оценить изменения на боковой стенке левого желудочка;
- aVF (усиленное от правой ноги) — задняя часть диафрагмальной поверхности;
- aVR (усиленное от правой руки) — считается малоинформативным, однако может использоваться для оценки инфарктных изменений в межжелудочковой перегородке и нижне-боковых отделах левого желудочка.
Грудные отведения:
- V1, V2 — изменения в межжелудочковой перегородке;
- V3 — передняя стенка;
- V4 — верхушечная локализация инфаркта;
- V5, V6 — боковая часть левого желудочка.
Передний или переднеперегородочный
При такой локализации поражения на кардиограмме изменения оценивают следующим образом:
- в I,II стандартном и aVL отведениях наблюдается зубец Q и единый с зубцом Т сегмент ST;
- в III стандартном и aVF отведениях — переход ST в расположенный ниже линии Т-зубец;
- в 1,2,3 грудных, а также при переходе на 4 грудное — отсутствие R и расположение ST выше линии на 0,2-0,3 см и более;
- отведения aVR и 4,5,6 грудные покажут следующие изменения: зубец Т уплощен, ST смещен вниз.
Боковой
ЭКГ при инфаркте с боковой локализацией сопровождается расширением и углублением Q-зубца, повышением ST и соединением этого сегмента с Т-зубцом. Эти признаки наблюдаются в III стандартном, 5,6 грудном и aVF отведениях.
Инфаркт на ЭКГ при диафрагмальной локализации имеет признаки:
- II, III и aVF отведения: широкий Q, положительный Т, соединенный с высоким ST;
- I отведение: опустившийся ниже линии ST;
- в некоторых случаях во всех грудных отведениях видны изменения зубца Т в виде отрицательной деформации и снижение ST.
Межжелудочковой перегородки
Поражение межжелудочковой перегородки инфарктом на ЭКГ проявляется углублением Q, подъемом Т и ST в отведениях, передающих информацию о состоянии передней части перегородки (I, aVL, 1,2 грудное). При ишемии в задней части перегородки (1 и 2 грудные отведения) видны: увеличенный зубец R, атриовентрикулярная блокада разных степеней и небольшое смещение ниже изолинии ST сегмента.

Передний субэндокардиальный
Этому виду инфаркта характерны изменения на ЭКГ:
- в I, aVL и 1-4 грудных отведениях — зубец Т положительный, высота его больше, чем у R;
- II, III стандартные — плавное снижение ST, отрицательное расположение зубца Т, низкий R;
- 5 и 6 грудные — разделение Т на отрицательную и положительную части.
Задний субэндокардиальный
При задней субэндокардиальной локализации признаки инфаркта миокарда на ЭКГ во II, III, aVF и 5, 6 грудном отведениях: зубец R уменьшается, Т становится положительным, а позже ST начинает опускаться.
Инфаркт правого желудочка
Т.к. у правого и левого желудочков общий источник кровоснабжения (коронарные артерии), при инфаркте в правой половине возникают изменения и в переднем отделе левого желудочка.
Диагностика с использованием электродов редко позволяет эффективно распознать правожелудочковый инфаркт даже с использованием дополнительных электродов. При этом типе нарушения кровообращения сердца показателям ЭКГ предпочтительна ультрасонография.
Несмотря на информативность метода, кардиограмма не является единственным тестом, на данные которого стоит опираться при диагностике инфаркта. Наряду с изменениями на кардиографической кривой учитываются клинические симптомы и показатели уровня кардиоспецифических ферментов: МВ-КФК, КФК, ЛДГ и др. Только наличие 2 и более признаков дает основание с точностью поставить диагноз.
28.04.2017
Инфаркт миокарда — одно из тяжелых заболеваний. Прогноз на прямую зависит от того, насколько правильно была проведена диагностика, и назначена адекватная терапия.
Чем раньше специалисты диагностируют заболевание, тем эффективнее будет лечение. Электрокардиография (ЭКГ) точнее всех исследований, именно она на 100% может подтвердить диагноз, либо же исключить его.
Сердечная кардиограмма
Человеческие органы пропускают слабый ток. Именно это, и позволяет с помощью прибора, который регистрирует электрические импульсы, поставить точный диагноз. Электрокардиограф состоит из:
- приспособления, усиливающего слабый ток;
- приспособления, измеряющего напряжение;
- записывающего устройства на автоматической основе.
По данным кардиограммы, которая выводится на экран или печатается на бумаге, специалист и ставит диагноз.
В сердце человека есть особые ткани, по другому их называют проводящей системой, они передают мышцам сигналы, указывающие на расслабление или сокращение органа.
Электрический ток в сердечных клетках поступает периодами, это:
- деполяризация. Отрицательный клеточный заряд сердечных мышц заменяется положительным;
- реполяризация. Восстанавливается отрицательный внутриклеточный заряд.
Поврежденная клетка имеет низкую электропроводность, чем здоровая. Именно это и фиксирует электрокардиограф.
Прохождение кардиограммы позволяет записать действие токов, которые возникают в работе сердца.
Когда ток отсутствует, то гальванометр фиксирует ровную линию (изолиния), а если клетки миокарда возбуждаются в разных фазах, то гальванометр фиксирует характерный зубец, направленный вверх или вниз.
Электрокардиографическая проверка фиксирует три стандартных отведения, усиленных три и грудных шесть. Если есть показания, то еще добавляют отведения, чтобы проверить задние сердечных отделы.
Каждое отведение электрокардиограф фиксирует отдельной линией, что в дальнейшем помогает диагностировать сердечные поражения.
В итоге комплексная кардиограмма имеет 12 графических линий, и каждая из них изучается.
На электрокардиограмме выделяются пять зубцов — P, Q,R,S,T, бывают случаи, когда добавляют еще и U. У каждого своя ширина, высота и глубина, а также направлен каждый в своем направлении.
Между зубцами есть интервалы, они тоже измеряются и изучаются. Также фиксируют интервальные отклонения.
Каждый зубец отвечает за функции и возможности определенных мышечных отделов сердца. Специалисты учитывают соотношение между ними (все зависит от высоты, глубины и направления).
Все эти показатели помогают отличить нормальную работу миокарда от нарушенной, вызванной разными патологиями.
Главная особенность электрокардиограммы заключается в выявлении и регистрации важных для диагностики и дальнейшего лечения симптомов патологии.
Определение инфаркта на экг
Из-за того, что начинают отмирать участки мышц сердца, начинает местно снижаться электрические возможности сравнительно с оставшимися неповрежденными тканями.
Именно, это и указывает где конкретно локализуется инфаркт миокарда. Малейшие изменения на экг указывают пораженные участки миокарда, которые возникают при ишемических сердечных болезнях:
- омертвение клеток — как правило, это происходит в центре органа, изменяется комплекс Q, R, S. В основном, образуется болезненный зубец Q;
- поврежденная зона — локализуется вокруг омертвевших клеток, на экг заметно, что смещен сегмент S,T;
- зона со сниженным кровообращением — находится на черте с не пораженным миокардом. Изменяется амплитуда и полярность зубца Т.
Изменения на электрокардиограмме определяет глубину омертвления клеток сердечных мышц:
- трансмуральный инфаркт миокарда — на графическом изображении выпадает зубец R, и вместо комплекса Q,R,S получается Q.S;
- субэпикардиальный инфаркт миокарда — указывает на сегментарную депрессию S, T. причем изменяется сам зубец Т, при этом комплекс Q, R, S — не меняется;
- интрамуральный инфаркт миокарда сопровожден изменениями Q, R, S и высотой сегмента S, T, который сопровождается слиянием с положительным зубцом Т.
Признаки инфаркта миокарда на экг имеет три этапа развития:
- первый этап может длиться от пару часов до 68 (трое суток). При проведении электрокардиограммы специалисты замечают, что сегмент ST поднимается (получается подъем в виде купола) и сливается с положительным зубцом. Сегмент начинается низко сходящего зубца. В этом случае на изображении появляется зубец Q, он считается патологическим.
- второй этап, подострый. Может длиться около месяца, иногда и двух. На кардиограмме фиксируется сниженный сегмент S, T и он приближается к изолинии. Формируется отрицательный зубец Т и увеличивается патологический Q.
- третий этап — рубцовый. Может длиться очень долго. Миокард имеет вид постинфарктного кардиосклероза и его могут фиксировать на электрокардиограмме на протяжении всей жизни у пациента, который перенес инфаркт. Рубцовый этап изображается на экг в виде сниженного сегмента S, T. Он снижается до уровня изолинии и формирует негативный характерный зубец Т, который имеет треугольный вид. Зубец Q остается неизменным. Через некоторое время он не исчезает, а просто сглаживается, и постоянно определяется врачами.
 У большинства пациентов сердечная динамика на электрокардиограмме не совпадает с морфологическим изменение мышц сердца.
У большинства пациентов сердечная динамика на электрокардиограмме не совпадает с морфологическим изменение мышц сердца.
Например, при проведении экг, врачи определили рубцовый этап развития инфаркта, но при этом рубцовая ткань еще не начала формироваться.
Или наоборот, второй этап (подострый) определяется на электрокардиограмме несколько месяцев, при этом рубец уже окончательно сформированный.
Поэтому при постановке диагноза, врачи учитывают не только расшифровку кардиограммы и стадии инфаркта, но и клинические проявления патологии и результаты лабораторных исследований.
Как определить где локализуется инфаркт на экг
Практически во всех случаях при уменьшенном кровоснабжении инфаркт локализуется в левом желудочке мышечного слоя сердца, справа — диагностируется в редких случаях. Поражается передняя, боковая и задняя часть.
При проведении ЭКГ признаки инфаркта миокарда определяются в отведениях:
- Ишемическая болезнь сердца в передней части указывает на нарушения в отведениях груди — V1, V2, V3, 1 и 2 — это нормальный показатель, а в усиленном случае AVL.
- Ишемия на боковых стенках отдельно диагностируется редко, чаще локализуется на передних и задних стенках левого желудочка, нарушения заметны в отведениях V3, V4, V5 в дополнении с 1 и 2 нормальными показателями, а в усиленном случае AVL.
- Ишемия на задней стенке имеет два вида: диафрагмальный (патологические нарушения определены отведении усиленного характера AVF, также затрагивается второе и третье отведение; базальный — увеличивается зубец R в левом отведении грудины.
Ишемическая болезнь сердца в области правого желудочка и предсердия диагностируются в редких случаях, в основном, прикрываются признаками сердечных поражений в левом отделе.
Может ли кардиограмма определить обширность инфаркта
На распространенность сердечных поражений указывают изменения в отведениях. По этим данным различают два вида инфаркта миокарда:
- Мелкоочаговый указывает на отрицательные показатели Т, при этом смещен сегментальный интервал S, T, а патологические резцы R, Q не наблюдаются.
- Распространенный вызван всеми измененными отведениями.
Определение глубины омертвения мышечного слоя
Инфаркт различается по глубине омертвения сердечных стенок:
- субэпикардиальный — поражается зона под наружным сердечным слоем;
- субэндокардиальный — омертвение происходит возле внутреннего слоя;
- трансмуральный — поражается вся толща миокарда.
Проведенная кардиограмма при инфаркте всегда определяет глубину некроза.
Сложности при электрокардиографии

Современная медицина и новые аппараты ЭКГ в состоянии легко проводить расчеты (это происходит автоматически). С помощью холтеровского мониторирования можно фиксировать работу сердца на протяжении суток.
В современных палатах стоит кардиомониторное наблюдение и имеет звуковой сигнал тревоги, это позволяет врачами замечать измененные сердечные сокращения.
Окончательный диагноз ставится специалистом по результатам электрокардиограммы, клинических проявлений.
Инфаркт миокарда: общие принципы ЭКГ диагностики.
При инфаркте (некрозе) мышечные волокна погибают. Некроз, как правило, обусловлен тромбозом коронарных артерий или их длительным спазмом, или стенозирующим коронаросклерозом. Зона некроза не возбуждается и не образует ЭДС. Некротический участок как бы пробивает окно внутрь сердца, и при трансмуральном (на всю глубину) некрозе на субэпикардиальную зону проникает внутриполостной потенциал сердца.
В абсолютном большинстве случаев у человека поражаются артерии, питающие левый желудочек, и потому инфаркты возникают в левом желудочке. Инфаркт правого желудочка возникает несравнимо реже (менее 1%случаев).
Электрокардиограмма позволяет не только диагностировать инфаркт (некроз) миокарда, но и определить его локализацию, величину, глубину некроза, стадию процесса и некоторые осложнения.
При резком нарушении коронарного кровотока в мышце сердца последовательно развиваются 3 процесса: гипоксия (ишемия), повреждение и, наконец, некроз (инфаркт). Длительность предварительных инфаркту фаз зависит от многих причин: степени и скорости нарушения кровотока, развития коллатералей и др. но обычно они длятся от нескольких десятков минут, до нескольких часов.
Процессы ишемии и повреждения изложены в на предыдущих страницах пособия. Развитие некроза сказывается на сегменте QRS электрокардиограммы.
Над участком некроза активный электрод регистрирует патологический зубец Q (QS).
Напомним, что у здорового человека в отведениях, отражающих потенциал левого желудочка (V5-6, I, aVL), может регистрироваться физиологический зубец q, отражающий вектор возбуждения перегородки сердца. Физиологический зубец q в любых отведениях, кроме aVR, не должен быть более 1/4 зубца R, с которым он записан, и продолжительнее 0.03 с.
При возникновении трансмурального некроза в мышце сердца над субэпикардиальной проекцией некроза регистрируется внутриполостной потенциал левого желудочка, который имеет формулу QS, т.е. представлен одним большим отрицательным зубцом. Если, наряду с некрозом, имеются и функционирующие волокна миокарда, то желудочковый комплекс имеет формулу Qr или QR. причем чем больше этот функционирующий слой, тем выше зубец R. Зубец Q в случае некроза имеет свойства зубца некроза: более 1/4 зубца R по амплитуде и продолжительнее 0.03с.
Исключением является отведение aVR, в котором в норме регистрируется внутриполостной потенциал, и потому ЭКГ в этом отведении имеет формулу QS, Qr или rS.
Еще одно правило: зубцы Q раздвоенные или имеющие зазубрины чаще всего патологические и отражают некроз (инфаркт миокарда).
Посмотрите на анимациях формирование электрокардиограммы при трех последовательных процессах: ишемии, повреждении и некрозе
Ишемия:
Повреждение:

Некроз:

Итак, на основной вопрос диагностики некроза (инфаркта) миокарда получен ответ: при трансмуральном некрозе электрокардиограмма в отведениях, которые находятся над зоной некроза, имеет формулу желудочного комплекса QS ; при нетрансмуральном некрозе желудочковый комплекс имеет вид Qr или QR .

Еще одна важная закономерность характерна для инфаркта: в отведениях, находящихся в зоне противоположной от очага некроза, регистрируются зеркальные (реципрокные, дискардантные) изменения — зубцу Q соответствует зубец R, а зубцу r(R) — зубец s(S). Если над зоной инфаркта сегмент ST приподнят дугой вверх, то на противоположных участках он опущен дугой вниз (См. рисунок).
Локализация инфаркта.
Электрокардиограмма позволяет различать инфаркт задней стенки левого желудочка, перегородки, передней стенки, боковой стенки, базальной стенки левого желудочка.
Ниже приведена таблица диагностики разной локализации инфаркта миокарда по 12 отведениям, входящим в стандарт электрокардиографического исследования.
+ Средства лечения
Инфаркт миокарда
Различные отведения ЭКГ в топической диагностике очаговых изменений миокарда. На всех этапах развития ЭКГ, начиная с применения В. Эйнтговеном (1903) трех классических (стандартных) отведений, исследователи стремились дать практическим врачам простой, точный и наиболее информативный метод регистрации биопотенциалов сердечной мышцы. Постоянный поиск новых оптимальных методик регистрации электрокардиограммы привел к значительному увеличению отведений, число которых продолжает возрастать.
В основу регистрации стандартных отведений ЭКГ положен треугольник Эйнтговена, углы которого образуют три конечности: правая и левая руки и левая нога. Каждая сторона треугольника образует ось отведения. Первое отведение (I) формируется за счет разности потенциалов между электродами, наложенными на правую и левую руки, второе (II)—между электродами правой руки и левой ноги, третье (III) —между электродами левой руки и левой ноги.
При помощи стандартных отведений можно выявлять очаговые изменения как в передней (I отведение), так и в задней стенке (III отведение) левого желудочка сердца. Однако, как показали дальнейшие исследования, стандартные отведения в ряде случаев либо совсем не выявляют даже грубых изменений миокарда, либо изменения графики отведений приводят к ошибочной диагностике очаговых изменений. В частности, изменения в базально-боковых отделах левого желудочка не всегда отражаются в I отведении, базально-задних — в III отведении.
Глубокий зубец Q и отрицательный зубец Т в III отведении могут быть и в норме, однако на вдохе эти изменения исчезают или уменьшаются, отсутствуют в таких дополнительных отведениях, как avF, avL, D и Y. Отрицательный зубец Т может быть выражением гипертрофии и перегрузки, в связи с чем заключение дается по совокупности изменений, обнаруживаемых в различных отведениях электрокардиограммы.
Поскольку регистрируемый электрический потенциал увеличивается по мере приближения электродов к сердцу, а форма электрокардиограммы в большей мере определяется электродом, расположенным на грудной клетке, то вскоре за стандартными стали применять .
Принцип регистрации этих отведений заключается в том, что дифферентный (основной, регистрирующий) электрод располагается м грудных позициях, а индифферентный — на одной из трех конечностей (на правой или левой руке, или левой ноге). В зависимости пт расположения индифферентного электрода различают грудные отведения CR, CL, CF (С — chest — грудь; R — right — правый; L — link —левый; F — foot — нога).
Особенно длительное время в практической медицине пользовались CR-отведениями. При этом один электрод помещали на правую руку (индифферентный), а другой (дифферентный, регистрирующий) в области груди в позициях от 1 до 6 или даже до 9 (CR 1-9). В I-й позиции дифферентный электрод накладывали на область четвертого межреберья по правому краю грудины; во 2-й позиции — па четвертое межреберье по левому краю грудины; в 3-й позиции — посередине линии, соединяющей 2-ю и 4-ю позиции; в 4-й позиции — на пятое межреберье по срединно-ключичной линии; в 5-й, 6-й и 7-й позициях — по передней, средней и задней подмышечных линиях на уровне 4-й позиции, в 8-й и 9-й позициях — по среднелопаточной и паравертебральной линиям на уровне 4-й позиции. Эти позиции, как это будет видно ниже, сохранились и в настоящее время и применяются для регистрации ЭКГ по Вильсону.
Однако в дальнейшем было установлено, что как сам индифферентный электрод, так и место расположения его на различных конечностях оказывают влияние на форму электрокардиограммы.
Стремясь свести к минимуму влияние индифферентного электрода, Ф. Вильсон (1934) объединил три электрода от конечностей в один и подключил его к гальванометру через сопротивление 5000 Ом. Создание такого индифферентного электрода с «нулевым» потенциалом позволило Ф. Вильсону разработать однополюсные (униполярные) отведения от грудной клетки и конечностей. Принцип регистрации этих отведений заключается в том, что вышеупомянутый индифферентный электрод подсоединяется к одному полюсу Гальванометра, а к другому полюсу подключается дифферентный электрод, который накладывается в перечисленных выше грудных позициях (V 1-9 . где V — volt) или на правую руку (VR), левую руку (VL) и левую ногу (VF).
При помощи вильсоновских грудных отведений можно определить локализацию поражений миокарда. Так, отведения V 1-4 отражают изменения в передней стенке, V 1-3 — в переднесептальной области, V 4 — в области верхушки, V 5 — в передней и частично в боковой стенке, V 6 — в боковой стенке, V 7 — в боковой и частично в задней стенке, V 8-9 —в задней стенке и межжелудочковой перегородке. Однако отведения V 8-9 широко не применяются из-за неудобства наложения электродов и малой амплитуды зубцов электрокардиограммы. Не нашли практического применения и отведения от конечностей по Вильсону из-за низкого вольтажа зубцов.
В 1942 г. отведения от конечностей по Вильсону были модифицированы Е. Гольбергером, предложившим в качестве индифферентного электрода использовать объединенный в один узел провод от двух конечностей без дополнительного сопротивления, а свободный провод от третьей конечности является дифферентный электродом. При этой модификации амплитуда зубцов увеличилась в полтора раза по сравнению с одноименными отведениями по Вильсону. В связи с этим отведения по Гольбергеру стали называться усиленными (а — augmented — усиленный) однополюсными отведениями от конечностей. Принцип регистрации отведений Заключается в том, что дифферентный электрод поочередно накладывают на одну из конечностей: правую руку, левую руку, левую ногу, а провода от остальных двух конечностей объединяются в один индифферентный электрод. При наложении дифферентного электрода на правую руку регистрируется отведение aVR, на левую руку — avL и левую ногу — avF. Внедрение этих отведений в практику значительно расширило возможности электрокардиографии в диагностике сердечно-сосудистых заболеваний. В отведении avR наилучшим образом отражаются изменения правого желудочка и предсердия. Отведения avL и avF незаменимы при определении позиции сердца. Отведение avL имеет важное значение также для диагностики очаговых изменений в базально-боковых отделах левого желудочка, отведение avF — в задней стенке, в частности в диафрагмальной ее части.
В настоящее время обязательна регистрация ЭКГ в 12 отведениях (I, II, III, avR, avL, avF, V 1-6).
Однако в ряде случаев диагностика очаговых изменений по 12 общепринятым отведениям затруднительна. Это побудило ряд исследователей к поиску дополнительных отведений. Так, иногда пользуются регистрацией грудных отведений в аналогичных позициях от более высоких межреберий. Тогда отведения обозначаются так: сверху указывается межреберье, а снизу — позиция грудного электрода (например, V 2 2 . У 2 3 т.д.), или с правой половины грудной КЛеТКИ V 3R —V 7R .
К более широко применяемым дополнительным отведениям относятся двухполюсные грудные отведения по Нэбу. Предложенная им техника регистрации отведений заключается в том, что электрод от правой руки помещается во втором межреберье справа у края грудины, электрод от левой руки — по задней подмышечной линии на уровне проекции верхушки сердца (V 7), электрод от левой ноги — на месте верхушечного толчка (V 4). При установке переключателя отведений на I контакте регистрируется отведение D (dorsalis), на II контакте — A (anterior) и на III контакте I (inferior). Этими отведениями достигается не плоское, а топографическое отображение потенциалов трех поверхностей сердца: задней, передней и нижней.
Ориентировочно отведение D соответствует отведениям V 6-7 и отражает заднюю стенку левого желудочка; отведение А соответствует отведениям V 4—5 и отражает переднюю стенку левого желудочка; отведение I соответствует отведениям У 2-3 и отражает межжелудочковую перегородку и частично переднюю стейку левого желудочка.
По данным В. Нэба, в диагностике очаговых изменений отведение D более чувствительно для заднебоковой стенки, чем отведения III, avF и V 7 . а отведения А и I более чувствительны, чем грудные отведения по Вильсону в диагностике очаговых изменения передней стенки. По данным В. И. Петровского (1961, 1967), отведение D не реагирует на очаговые изменения в диафрагмальной области. При отрицательном зубце Т, который обнаруживается в III отведении в норме и при горизонтальной позиции сердца, наличие положительного зубца Т в отведении D исключает патологию.
По нашим данным, независимо от позиции сердца регистрация отведения D обязательна при наличии отрицательного зубца Т, а также глубокого, даже не уширенного зубца Q в III отведения и отсутствии подобных изменений в avF. Отведение avF отражает преимущественно заднедиафрагмальные отделы левого желудочка, И опадение D — задиебазальные (базально-боковые). Поэтому мел-(И)очшовые изменения в базальных отделах левого желудочка отражаются в отведении D и могут отсутствовать в avF, а сочетание Изменений в отведениях D и avF указывает на более распространимте поражение задней стенки левого желудочка.
Отведение V E (Е — ensiformis — септальное) регистрируется грудное отведение, но при установке дифферентного электрода в области мечевидного отростка. Отведение отражает очаговые изменения в перегородочной области. Им пользуются при нечетких изменениях в отведениях V 1-2 .
Диагностика ограниченных очаговых изменений в базально-боковых отделах левого желудочка, когда процесс не распространился ни переднюю и заднюю стенки, нередко становится невозможной при использовании 12 общепринятых отведений. В этих случаях заслуживает внимания регистрация полусагиттальных отведении по методике Слапак а — Портилла . Поскольку эти отведения являются модификацией отведения D по Нэбу, то индифферентный электрод от левой руки помещается в позицию V 7 . а дифферентный электрод от правой руки перемещается по линии, соединяющей две точки: одна — во втором межреберье слева от грудины, вторая — во втором межреберье по передней подмышечной линии.
ЭКГ регистрируют в следующих позициях:
S 1 — дифферентный электрод во втором межреберье слева от грудины;
S 4 — по передней подмышечной линии на уровне S 1 ;
S 2 и S 3 — на равном расстоянии между двумя крайними точками (между S 1 и S 4).
Переключатель отведений устанавливается на I контакте. Эти отведения регистрируют очаговые изменения в базально-боковых отделах левого желудочка. К сожалению, графика этих отведений в определенной степени зависит от формы грудной клетки и анатомического положения сердца.
В последние два десятилетия в практической электрокардиографии стали применять ортогональные двухполюсные некорригированные и корригированные отведения.
Оси отведений ортогональной электрокардиограммы направлены в трех взаимно перпендикулярных плоскостях: горизонтальной (X), фронтальной (G) и сагиттальной (Z).
Ортогональное двухполюсное некорригированное отведение X образуется двумя электродами: положительным (с левой руки), который помещается в позицию V 6 . и отрицательным (с правой руки) — в позицию V 6R . Отведение Z регистрируется при положении положительного (с левой руки) электрода в позиции V 2 и отрицательного (с правой руки) в позиции V 8R .
Отведение V регистрируется при наложении положительного электрода (с левой руки) на область мечевидного отростка и отрицательного (с правой руки) — во второе межреберье справа у грудины. Наконец, к приведенным отведениям приближается отведение R 0 . которое регистрируется при наложении положительного (с левой руки) электрода в позиции V 7 . отрицательного (с правой руки) — в позиции V1.
Отведения регистрируются в положении переключателя отведений на I контакте.
Ориентировочно отведение X соответствует отведениям I, avL V 5-6 и отражает переднебоковую стейку левого желудочка. Отведениє V соответствует отведениям III и avF и отражает заднюю стенку. Отведение Z соответствует отведению V 2 и отражает меж-желудочковую перегородку. Отведение Ro соответствует отведениям V 6-7 и отражает заднебоковую стенку левого желудочка.
При крупноочаговом инфаркте миокарда, независимо от его локализации, в левом желудочке ортогональные отведения всегда реагируют соответствующей графикой, в то время как при мелкоочаговых поражениях миокарда, особенно в базальных отделах левого желудочка, изменения в этих отведениях часто отсутствуют. В таких случаях используются отведения по Слапаку—Портилла и грудные отведения от более высоких межреберий.
Корригированные ортогональные отведения основаны на строгих физических принципах с учетом эксцентричности и изменчивости сердечного диполя, а потому малочувствительны к индивидуальным особенностям грудной клетки и анатомическому положению сердца.
Для регистрации корригированных ортогональных отведений предложены различные комбинации соединенных между собой через определенные сопротивления электродов.
При наиболее часто применяемых корригированных ортогональных отведениях по Франку электроды размещаются следующим образом: электрод Е — на грудине на уровне между четвертым-пятым межреберьем, электрод М — сзади на уровне электрода Е, электрод А — по левой средней подмышечной линии на уровне электрода Е, электрод С — под углом 45° между электродами А и Е, т. е. посередине линии, соединяющей точки электродов А и Е, электрод F — по правой средней подмышечной линии на уровне электрода Е, электрод Н — на задней поверхности шеи и электрод F — на левой ноге. На правую ногу закладывается заземленный электрод. Таким образом, по системе Франка электроды Е, М, А, С, I размещаются по кругу туловища на уровне прикрепления V ребра к грудине.
В практической медицине корригированные отведения применяются редко.
В литературе приводятся и другие дополнительные отведения: ЗР по Пескодору; Dm, Am, Im, CKR, CKL, CKF по Гуревичу и Крынскому; MCL, и MCL 6 по Марриоту. Однако они не имеют значительных преимуществ перед приведенными выше и в практической медицине не используются.
В настоящее время большое значение придается определению размеров очагового повреждения миокарда неинвазивными методами, что важно как для ближайшего и отдаленного прогноза заболевания, так и для оценки эффективности методов лечения, направленных на ограничение зоны ишемического повреждения. Для этой цели регистрируется электрокардиотопограмма. При этом предложено использовать различное количество прекардиальных отведений. Наибольшее распространение получила система из 35 отведений с пятью горизонтальными рядами от второго до шестого межреберий включительно и семью вертикальными (по правой и левой окологрудинным линиям, середине расстояния между левой окологрудинной и левой срединно-ключичной линиями, по левой срединно-ключичной, передней, средней и задней подмышечным линиям). Запись ЭКГ проводится по Вильсону с использованием грудного электрода. Исходя из представлений о том, что отведения, в которых регистрируются подъемы сегмента S—Т, соответствуют периинфарктной зоне, в качестве показателя размеров зоны ишемического повреждения миокарда P. R. Магоко с соавторами (1971) предложили индекс NST (количество отведений с подъемом сегмента S—Т более 1,5 мм), в качестве показателя тяжести повреждения — частное от деления суммы подъемов S—Т в мм на NST (ST = ΣST/NST). Количество отведений ЭКГ, в которых определялись подъемы сегмента S—Т и изменения желудочкового комплекса но типу QS, изображают с помощью картограммы, где каждое из 35 отведений условно представляется квадратом площадью 1 см2 (Г В. Рябинина, 3. 3. Дорофеева, 1977). Конечно, выражаемую таким образом величину периинфарктной зоны и трансмурального пораження миокарда из-за разной толщины и конфигурации грудной клетки и положения сердца нельзя полностью отождествлять с реальными размерами соответствующих зон повреждения миокарда.
Недостатком метода электрокардиотопограммы является то, что его можно использовать лишь при локализации инфаркта миокарда н области передней и боковой стенок при отсутствии значительных нарушений внутрижелудочковой проводимости (блокады ножек пучка Гиса) и перикардита.
Таким образом, в настоящее время существуют разнообразные системы отведений и отдельные отведения ЭКГ, которые имеют большое диагностическое значение для определения характера и локализации очаговых изменений миокарда. При подозрении на наличие такого поражения обязательна регистрация следующих отведений: трех стандартных, трех усиленных с конечностей по Гольбергеру, шести грудных по Вильсону, трех по Нэбу и трех некорригированных ортогональных.
В неясных случаях, в зависимости от локализации зоны поражения, дополнительно регистрируются отведения V 7-9 . V E . R o . а иногда также S 1 -4 по Слапаку—Портилла, V 3R -6 R и V 1-7 в межреберьях выше и ниже пятого.
Hfpkbxyst jtdtltybz ‘RU d tjgbxtcrjq lbfuyjctbrt jxfujds[ bpvtytybq vbjrfhlf. Yf dct[ ‘tfgf[ hfpdbtbz ‘RU, yfxbyfz c ghbvtytybz D. ‘qytujdtyjv (1903) tht[ rkfccbxtcrb[ (ctfylfhtys[) jtdtltybq, bccktljdfttkb cthtvbkbcm lftm ghfrtbxtcrbv dhfxfv ghjctjq, tjxysq b yfb,jktt byajhvftbdysq vttjl htubcthfwbb ,bjgjttywbfkjd cthltxyjq vsiws. Gjctjzyysq gjbcr yjds[ jgtbvfkmys[ vttjlbr htubcthfwbb ‘ktrthjrfhlbjuhfvvs ghbdtk r pyfxbttkmyjve edtkbxtyb. jtdtltybq, xbckj rjtjhs[ ghjljk;ftt djphfctftm. D jcyjde htubcthfwbb ctfylfhtys[ jtdtltybq ‘RU gjkj;ty thteujkmybr ‘qytujdtyf, euks rjtjhjuj j,hfpe.t thb rjytxyjctb: ghfdfz b ktdfz herb b ktdfz yjuf. Rf;lfz ctjhjyf thteujkmybrf j,hfpett jcm jtdtltybz. Gthdjt jtdtltybt (I) ajhvbhettcz pf cxtt hfpyjctb gjttywbfkjd vt;le ‘ktrthjlfvb, yfkj;tyysvb yf ghfde. b ktde. herb, dtjhjt (II)—vt;le ‘ktrthjlfvb ghfdjq herb b ktdjq yjub, thttmt (III) —vt;le ‘ktrthjlfvb ktdjq herb b ktdjq yjub. Ghb gjvjob ctfylfhtys[ jtdtltybq vj;yj dszdkztm jxfujdst bpvtytybz rfr d gthtlytq (I jtdtltybt), tfr b d pflytq cttyrt (III jtdtltybt
Определение локализации инфаркта миокарда. Топография инфаркта миокарда по ЭКГ
Перед тем как приступить к описанию различных ЭКГ вариантов инфаркта . определяемых различиями в анатомической локализации, уместно вспомнить о том, что вкратце упоминалось в начале этой главы в отношении пораженных зон и коронарного кровообращения.
На рисунке показана схема различных петель QRS при различных локализациях инфаркта в соответствии с применяемой в кардиологической клинике Барселонского университета классификацией. Следует отметить, что электрокардиографические, ангиографические и патологоанатомические исследования показали, что если ЭКГ относительно специфична в предсказании локализации инфаркта, особенно при изолированном инфаркте (т. е. зубец Q в определенных отведениях довольно хорошо коррелирует с патологоанатомическими данными), ее чувствительность довольно низка (патологоанатомический инфаркт часто наблюдается при отсутствии аномального зуба Q на ЭКГ).
В целом чувствительность 12 отведений ЭКГ в диагностике ранее перенесенного инфаркта составляет около 65%, а специфичность варьирует от 80 до 95%. Существуют отдельные критерии, которые обладают малой чувствительностью (менее 20%), но высокой специфичностью. Более того, несмотря на значение ЭКГ в диагностике инфаркта, она неточно определяет его степень. Чувствительность отдельных критериев очень невелика, но возрастает в комбинации с несколькими другими методиками. Как будет вицно из дальнейшего изложения при различных типах инфаркта, ВКГ иногда располагает более чувствительными критериями. Например, переход инфаркта передней стенки на боковую или нижнюю стенку часто остается незамеченным. ВКГ может расширить диагностические возможности, как, например, при сомнительных зубцах Q, и выявить наличие нескольких некротизированных зон.
Врач должен попытаться оценить локализацию инфаркта по ЭКГ, даже несмотря на то, что не всегда имеет место взаимосвязь ЭКГ и патоморфологических изменений. Он также обязан Нижняя стенка является по существу, верхним отделом задней стенки. Инфаркт может быть классифицирован как трансмуральный или нетрансмуральный в зависимости от глубины поражения стенки; верхушечный или базальный в зависимости от высокой или низкой локализации; задний, передний, перегородочный или боковой в зависимости от области поражения стенки.

Инфаркт не всегда ограничивается исключительно перегородочной, передней, задней, нижней или боковой стенкой. Гораздо чаще встречаются различные комбинированные поражения, в целом зависящие от зоны поражения миокарда, что в свою очередь связано с окклюзией коронарной артерии.
Инфаркт обычно захватывает или переднеперегородочную (обычно вследствие окклюзии передней нисходящей коронарной артерии), или нижнезаднюю зону (вследствие окклюзии огибающей и/или правой коронарной артерии) левого желудочка. Боковая стенка сердца может быть повреждена в любой области. Инфаркт может быть более выраженным в той или другой зоне. В любом случае следует помнить о следующих обобщениях:
а) инфаркт обычно не поражает базальную часть передне-боковой перегородочной области;
б) инфаркт самой высокой части и заднебоковой, базальной стенки и/или межжелудочковой перегородки не сопровождается зубцами Q, указывающими на поражение, но может изменять конфигурацию конечной части петли;
в) в 25% случаев инфаркт задней стенки левого желудочка переходит на правый желудочек;
г) нижняя часть базальной половины задней стенки - это зона, которая соответствует классическому инфаркту задней стенки (высокий R в отведении V1, V2), в виде зеркального изображения в отведениях на спине, инфаркт задней стенки обычно не бывает изолированным, а поражает верхушечную часть задней стенки (нижнюю или диафрагмаль-ную).
Область миокарда, в которой развивается ИМ, зависит от расположения окклюзированной коронарной артерии и степени коллатерального кровотока. Имеется две главные системы кровоснабжения миокарда, одна кровоснабжает правую половину сердца, другая - левую половину.
Правая коронарная артерия проходит между правым предсердием и правым желудочком и затем загибается на заднюю поверхность сердца. У большинства людей она имеет нисходящую ветвь, которая кровоснабжает АВ-узел.
Левая коронарная артерия делится на левую нисходящую и левую огибающую артерии. Левая нисходящая артерия кровоснабжает переднюю стенку и большую часть межжелудочковой перегородки. Огибающая артерия проходит между левым предсердием и левым желудочком и кровоснабжает боковую стенку левого желудочка. Приблизительно у 10% населения она имеет ветвь, которая поставляет кровь к АВ-узлу.
Локализация инфаркта важна в прогностических и терапевтических целях для определения зоны некроза.
Локализация инфаркта может быть сгруппирована в несколько анатомических групп. Это нижние, боковые, передние и задние инфаркты миокарда. Возможны комбинации этих групп, например переднебоковой ИМ, которые очень часто встречается.
| Четыре основных анатомических места ИМ. |
Почти все инфаркты миокарда вовлекают левый желудочек. Это не удивительно, потому что левый желудочек - самая крупная сердечная камера и испытывает наибольшую нагрузку. Поэтому он является самой уязвимой областью при нарушении коронарного кровоснабжения. Некоторые нижние ИМ также вовлекают часть правого желудочка.
Характерные электрокардиографические изменения ИМ регистрируются только в тех отведениях, которые находятся над или около места поражения.
· Нижний ИМ вовлекает диафрагмальную поверхность сердца. Он часто вызывается окклюзией правой коронарной артерии или ее нисходящей ветви. Характерные электрокардиографические изменения могут быть замечены в нижних отведениях II, III и aVF.
· Боковой ИМ вовлекает левую боковую стенку сердца. Он часто происходит из-за окклюзии левой огибающей артерии. Изменения будут встречаться в левых боковых отведениях I, aVL, V5 и V6.
· Передний ИМ вовлекает переднюю поверхность левого желудочка и обычно вызывается окклюзией левой передней нисходящей артерии. Любое из грудных отведений (V1 - V6) может показать изменения.
· Задний ИМ вовлекает заднюю поверхность сердца и обычно вызывается окклюзией правой коронарной артерии. К сожалению, нет отведений, которые располагаются над задней стенкой. Диагноз поэтому основывается на реципрокных изменениях в передних отведениях, особенно V1. Реципрокные изменения будут обсуждены позже.
Заметка: Анатомия коронарных артерий может заметно изменяться среди индивидуумов, и тогда точно предсказать, какой сосуд поражён, невозможно.
Нижние инфаркты
Нижний ИМ, как правило, является результатом окклюзии правой коронарной артерии или ее нисходящей ветви. Изменения встречаются в отведениях II , III и aVF . Реципрокные изменения могут быть заметны в передних и левых боковых отведениях.
Хотя при большинстве образований ИМ патологические зубцы Q сохраняются в течение всей жизни пациента, это не обязательно верно при нижних ИМ. В течение первого полугодия у 50% пациентов исчезают критерии патологических зубцов Q. Наличие маленьких зубцов Q в нижних отведениях может поэтому предполагать рубцовые изменения после ИМ. Помните, однако, что маленькие нижние зубцы Q также могут быть заметны в норме.
Боковые инфаркты
Боковой ИМ является результатом окклюзии левой огибающей артерии. Изменения могут быть заметны в отведениях I , aVL , V5 и V6 . Реципрокные изменения отмечаются в нижних отведениях.
Передние инфаркты
Передний ИМ - результат окклюзии левой передней нисходящей артерии. Изменения заметны в грудных отведениях (V1 - V6 ). Если поражена вся левая коронарная артерия, наблюдается переднебоковой ИМ с изменениями в грудных отведениях и в отведениях I и aVL. Реципрокные изменения отмечаются в нижних отведениях.
Передний ИМ не всегда сопровождается формированием зубца Q. У некоторых пациентов может быть только нарушена нормальная прогрессия зубца R в грудных отведениях. Как Вы уже знаете, в норме грудные отведения показывают прогрессивное увеличение высоты зубцов R от V1 к V5. Амплитуда зубцов R должна увеличиваться, по крайней мере, на 1 мВ в каждом отведении от V1 до V4 (и часто V5). Эта динамика может нарушиться при переднем ИМ, данных эффект называют замедленной прогрессией зубца R. Даже при отсутствии патологических зубцов Q, замедленная прогрессия зубца R может показать передний ИМ.
Замедленная прогрессия зубца R не является специфичной для диагноза переднего ИМ. Она также может быть замечена при правожелудочковой гипертрофии и у больных с хроническими заболеваниеми легких.
Задние инфаркты
Задний ИМ, как правило, является результатом окклюзии правой коронарной артерии. Поскольку ни одно из обычных отведений не лежит над задней стенкой, диагноз верифицируется по реципрокным изменениям в передних отведениях. Другими словами, поскольку мы не сможем найти элевацию сегмента ST и зубцы Q в задних отведениях (которых нет), мы должны найти депрессию сегмента ST и высокие зубцы R в передних отведениях, особенно в отведении V1. Задний ИМ - зеркальное отражение переднего ИМ на ЭКГ.
Нормальный комплекс QRS в отведении V1 состоит из маленького зубца R и глубокого зубца S; поэтому наличие высокого зубца R, особенно с депрессией сегмента ST, легко заметно. При наличии клинических признаков зубец R большей амплитуды, чем соответствующий зубец S, указывают на задний ИМ.
Другая полезная подсказка. Поскольку нижняя и задняя стенки обычно имеют общее кровоснабжение, задний ИМ часто сопровождается образованием инфаркта нижней стенки.
Одно напоминание: Наличие большого зубца R, превышающего амплитуду зубца S зубец в отведении V1, является также критерием диагноза правожелудочковой гипертрофии. Диагноз правожелудочковой гипертрофии, однако, требует наличия отклонения электрической оси вправо, которое отсутствует при заднем ИМ.
Какова локализация инфаркта? Действительно ли он острый?
Не-Q инфаркт миокарда
Не все инфаркты миокарда сопровождаются возникновением зубца Q. Ранее считалось, что зубцы Q регистрируются при проникновении ИМ на всю толщину миокардиальной стенки, тогда как отсутствие зубцов Q указывало на образование инфаркта только во внутреннем слое миокардиальной стенки, названной субэндокардом. Эти инфаркты назывались трансмуральными или субэндокардиальными.
Однако, исследования обнаружили отсутствие чёткой корреляции между появлением зубцов Q и глубиной поражения миокарда. При некоторых трансмуральных ИМ не наблюдаются зубцы Q, а при некоторых субэндокардиальных ИМ зубцы Q появляются. Поэтому старая терминология была заменена на термины "инфаркт с зубцом Q" и "инфаркт без зубца Q".
Единственными изменениями ЭКГ, замеченными при инфаркте миокарда без зубца Q, являются инверсия зубца T и депрессия сегмента ST.
Установлено, что при не-Q-ИМ имеется более низкая смертность и более высокий риск рецидива и летальности при Q-ИМ.
Стенокардия
Стенокардия - типичная боль в груди, связанная с ИБС. У пациента со стенокардией может развиться инфаркт миокарда или стенокардия может протекать стабильно много лет. ЭКГ, зарегистрированная во время приступа стенокардии, покажет депрессию сегмента ST или инверсию зубца T.
 |
| Три примера изменений ЭКГ, которые могут сопровождать стенокардию: (A) Инверсия зубца T; (B) Депрессия сегмента ST; и (C) Депрессия сегмента ST с инверсией зубца T. |
Важными отличиями депрессии сегмента ST при стенокардии и не-Q-ИМ являются клиническая картина и динамика. При стенокардии сегменты ST обычно возвращаются к основанию вскоре после того, как приступ стихает. При не-Q-ИМ сегменты ST остаются сниженными в течение по крайней мере 48 часов. Может быть полезно определение кардиальных ферментов, которые будут увеличены при формировании ИМ, и не изменяются при стенокардии.
Стенокардия Принцметала
Имеется один тип стенокардии, которая сопровождается элевацией сегмента ST. В отличии от типичной стенокардии, которая обычно провоцируется физической нагрузкой и является результатом прогрессивного атеросклеротического поражения коронарных артерий, стенокардия Принцметала может встречаться в любое время, и у многих пациентов является результатом спазма коронарной артерии. По-видимому, элевация сегмента ST отражает обратимое трансмуральное повреждение. У контуров сегментов ST часто не будет округленной, куполообразной формы, как при ИМ, и сегменты ST быстро возвращаются к основанию после купирования приступа.
Пациенты со стенокардией Принцметала фактически разделяются на две группы: без атеросклероза коронарных артерий, боль определяется исключительно спазмом коронарной артерии, и с атеросклеротическим поражением. ЭКГ не помогает различить эти две группы.
Резюме
Сегмент ST при ишемической болезни сердца
Элевация сегмента ST
Может быть заметна при развитии трансмурального инфаркта миокарда или при стенокардии Принцметала.
Депрессия сегмента ST
Может быть заметна при типичной стенокардии или инфаркте миокарда без зубца Q.
Форма сегмента ST у больных с острой ишемической болью является главным определяющим фактором при выборе терапии. Пациенты с острой элевацией сегмента ST на ЭКГ нуждаются в немедленной реперфузионной терапии (тромболизис или пластическая операция на сосудах). Пациенты с депрессией сегмента ST или без изменений сегмента ST обычно получают консервативную терапию.
Ограничения ЭКГ в диагностике инфаркта миокарда
Электрокардиографическая картина развивающегося инфаркта миокарда, как правило, включает изменения сегмента ST и появление новых зубцов Q. Любые факторы, которые маскирует эти эффекты, искажая сегмент ST и комплекс QRS, оказывают негативное влияние на электрокардиографическую диагностику ОИМ. Два из таких факторов - синдром WPW и блокада левой ножки пучка Гиса.
Правило : При блокаде левой ножки пучка Гиса или синдроме Вольффа-Паркинсона-Уайта диагноз инфаркта миокарда не может быть достоверным по ЭКГ. Это правило включает пациентов с блокадой левой ножки пучка Гиса на ЭКГ из-за желудочковой электрокардиостимуляции.
У больных с синдромом WPW, дельта-волны часто отрицательны в нижних отведениях (II, III и aVF). Эти изменения часто упоминаются как псевдоинфарктные, потому что дельта-волны могут напоминать зубцы Q. Короткий интервал PR - главная подсказка, по которой можно отличить WPW от ОИМ.
Тестирование с физической нагрузкой
Тестирование с физической нагрузкой является атравматичным методом оценки наличия ИБС. Этот метод небезупречен (ложноположительные и ложноотрицательные результаты встречаются в большом количестве), но это - один из лучших доступных скрининговых методов.
Тестирование с физической нагрузкой обычно выполняется пациентом на тредмиле путем однообразной шаговой ходьбы или на велотренажере. Пациент подключается к монитору ЭКГ и в течении процедуры непрерывно записывается полоса ритма. Полная ЭКГ с 12 отведениями регистрируется через короткие интервалы. Каждые несколько минут увеличиваются скорость и угол наклона шаговой ленты до появления следующих моментов: (1) пациент не может продолжать процедуру по любой причине; (2) достижение максимальной частоты сердечных сокращений пациента; (3) появление кардиальных симптомов; (4) появление существенных изменений на ЭКГ.
 |
Физиология оценки тестирования проста. Классифицированный протокол нагрузки вызывает безопасное и постепенное увеличение частоты сердечных сокращений пациента и систолического артериального давления. Артериальное давления пациента, умноженное на частоту сердечных сокращений, является хорошим показателем потребления миокардом кислорода. Если потребность миокарда в кислороде превышает возможность его доставки, на ЭКГ могут быть зафиксированы изменения, характерные для ишемии миокарда.
Значительное атеросклеротическое поражение одной или нескольких коронарных артерий ограничивает кровоснабжение миокарда и ограничивает потребление кислорода. Хотя ЭКГ в состоянии покоя может быть нормальной, при физической нагрузке могут быть зарегистрированы субклинические признаки ИБС.
При положительном тесте на ИБС ЭКГ покажет депрессию сегмента ST. Изменения зубца T являются слишком неопределенными, чтобы иметь клиническое значение.
При депрессии сегмента ST во время тестирования, особенно если изменения сохраняются несколько минут в период восстановления, высока вероятность наличия ИБС и поражения левой коронарной артерии или нескольких коронарных артерий. Появление кардиальных симптомов и снижение артериального давления - особенно важные признаки, при которых тестирование должно быть немедленно остановлено.
Уровень ложноположительных и ложноотрицательных результатов зависит от популяции населения, которая проверяется. Положительный анализ у молодого, здорового человека без симптомов и факторов риска ИБС, вероятно, будет ложноположительным. С другой стороны положительный анализ у пожилого человека с болью в груди, перенесённым ИМ, и артериальной гипертензией с высокой вероятностью будет истинно положительным. Отрицательный результат испытаний не исключают возможность ИБС.
Показания для тестирования с физической нагрузкой следующие:
· Дифференциальная диагностика болей в грудной клетке
· Обследование пациента, недавно перенёсшего ИМ, с целью оценки прогноза его заболевания и потребности в дальнейшем инвазивном тестировании, таком как катетеризация сердца
· Общая оценка пациентов старше 40 лет при наличии факторов риска ИБС.
Противопоказания включают любое острое заболевание, тяжелый аортальный стеноз, декомпенсированную застойную сердечную недостаточность, тяжелую артериальную гипертензию, стенокардию покоя, и наличие значительной аритмии.
Летальность от процедуры очень низка, но оборудование для сердечно-легочной реанимации должно всегда быть доступным.
Джоан Л. - 62-летний руководящий работник. Она находится в важной командировке и проводит ночь в отеле. Рано утром она просыпается с одышкой и тяжестью в грудной клетке, которая иррадиирует в нижнюю челюсть и левую руку, умеренным головокружением и тошнотой. Она встает с кровати, но боль не уходит. Она звонит в приемное отделение. Ее жалобы передаются по телефону доктору, обслуживающему отель, который немедленно приказывает, чтобы машина скорой помощи доставила ее в местное отделение неотложной помощи. Она прибывает туда спустя только 2 часа после появления ее симптомов, которые продолжаются несмотря на три принятых таблетки нитроглицерина.
В отделении неотложной помощи ЭКГ показывает следующее:
Имеется ли у неё инфаркт миокарда? Если ответ положительный, Вы можете сказать, острые ли это изменения и какая область сердца поражена?
Быстрое прибытие Джоан в отделение неотложной помощи, элевация сегментов ST, и отсутствие зубцов Q на ЭКГ означают, что она - превосходный кандидат или на тромболитическую терапию, или на острую коронарную пластическую операцию на сосудах. К сожалению, она только 1 месяц назад переболела геморрагическим инсультом, имеет легкий гемипарез слева, что препятствует тромболитической терапии. Кроме того, острая пластическая операция на сосудах недоступна в этой небольшой больнице, а самый близкий крупный медицинский центр на расстоянии в несколько часов. Поэтому Джоан была госпитализирована в кардиологическое отделение.
Поздно ночью одна из медсестер замечает специфические сокращения на ее ЭКГ:
ЭКГ Джоан показывает, что желудочковые эктопии были подавлены. Она также показывает появление новых зубцов Q в передних отведениях с последовательным полным развитием переднего инфаркта миокарда.
Позже днем, Джоан начинает вновь испытывать боль в груди. Снята повторная ЭКГ: Что изменилось?
У Джоаны развилась АВ-блокада третьей степени. Тяжёлые блокады проведения обычно встречаются при передних ИМ. Ее головокружение происходит из-за несоответствующей насосной функции миокарда при частоте сокращений желудочков в 35 уд/мин. Установка искусственного водителя ритма обязательна.
Последние штрихи
Имеется много медикаментов, нарушений электролитного обмена и других нарушений, которые могут существенно изменить нормальную структуру ЭКГ.
В некоторых из этих случаев ЭКГ может быть самым чувствительным индикатором угрожающей катастрофы. В других даже незначительные электрокардиографические изменения могут быть ранним признаком нарастающей проблемы.
Мы не будем останавливаться на механизмах этих изменений в этой главе. Во многих случаях причины изменений на ЭКГ просто не известны. Темы, которые мы затронем, включают следующие:
· Электролитные нарушения
· Гипотермия
· Медикаменты
· Другие кардиальные нарушения
· Заболевания легких
· Болезни центральной нервной системы
· Сердце атлета.
Электролитные нарушения
Изменения уровней калия и кальция могут значительно изменить ЭКГ.
Гиперкалиемия
Гиперкалиемия сопровождается прогрессивными изменениями на ЭКГ, которые могут достигнуть в высшей точке желудочковой фибрилляции и смерти. Наличие электрокардиографических изменений - более достоверный клинический признак калиевой токсичности, чем серологический калиевый уровень.
При увеличении калия начинают увеличиваться зубцы T во всех 12 отведениях. Этот эффект может быть легко перепутан с остроконечными зубцами T при остром инфаркте миокарда. Одно различие - изменения зубцов T при ОИМ ограничены теми отведениями, которые лежат над областью инфаркта, тогда как при гиперкалиемии, изменения диффузные.
При дальнейшем увеличении калия интервал PR удлиняется, а зубец P постепенно сглаживается и затем исчезает.
В дальнейшем комплекс QRS расширяется, затем он сливается с зубцом T, формируя синусоидальные комплексы. В конечном счете развивается желудочковая фибрилляция.
Важно отметить, что эти изменения не всегда соответствуют уровню калия в крови. Прогрессия изменений при гиперкалиемии до желудочковой фибрилляции может встречаться очень быстро. Любое изменение на ЭКГ из-за гиперкалиемии требует пристального клинического внимания.
Гипокалиемия
При гипокалиемии ЭКГ также может быть наилучшим признаком токсичности калия, чем его серологический уровень. Могут быть замечены три изменения, которые встречаются без определенного порядка:
· Депрессия сегмента ST
· Сглаживание зубца T
· Появление зубца U.
Термин зубец U дается зубцу, появляющемуся после зубца T в кардиальном цикле. Его точное физиологическое значение не полностью понятно. Хотя зубцы U - самая характерная особенность гипокалиемии, они не являются точным диагностическим признаком. Зубцы U иногда могут быть заметны в норме и при нормальном уровне калия.
Нарушения кальция
Изменения серологического уровня кальция прежде всего оказывают влияние на интервал QT. Гипокальциемия удлиняет его; гиперкальциемия сокращает его. Вы помните потенциально смертельную аритмию, связанную с удлинением интервала QT?
Веретенообразная желудочковая тахикардия, разновидность желудочковой тахикардии, отмечается у больных с удлинением интервала QT.
Гипотермия
При снижении температуры тела ниже 30°C встречаются несколько изменений на ЭКГ:
· Все замедляется. Распространена синусовая брадикардия, и все сегменты и интервалы (PR, QRS, QT) могут удлиниться.
· Может быть замечен отличительный и фактически диагностический тип элевации сегмента ST. Он состоит из резкого подъема прямо в точке J и затем внезапного снижения назад к основанию. Данную конфигурацию называют зубцом J или зубцом Осборна.
· В конечном счете могут возникнуть различные аритмии. Наиболее распространена предсердная фибрилляция с низкой ЧСС, хотя могут встречаться почти любые нарушения ритма.
· Мышечный тремор из-за дрожи может осложнить анализ ЭКГ. Подобный эффект может быть замечен у больных с болезнью Паркинсона. Не перепутайте его с трепетанием предсердий.
 |
| Помехи от мышечного тремора напоминают трепетание предсердий. |
Медикаменты
Сердечные гликозиды
Есть две категории электрокардиографических изменений, вызванных сердечными гликозидами: связанные с терапевтическими дозами лекарственного средства, и изменения при передозировке (токсичности) сердечными гликозидами.
Изменения ЭКГ, связанные с терапевтическими дозами СГ
Терапевтические дозы СГ характеризуются изменениями сегмента ST и зубца T у большинства пациентов. Эти изменения известны, как дигиталисный эффект, и состоят из депрессии сегмента ST со сглаживанием или инверсией зубца T. Снижение сегментов ST имеет косонисходящую форму, начинается почти сразу от зубца R. В этом отличие дигиталисного эффекта от более симметричной депрессии сегмента ST при ишемии. Более сложно дифференцировать дигиталисный эффект от желудочковой гипертрофии с расстройствами реполяризации, особенно потому, что СГ часто используются у больных с застойной сердечной недостаточностью, которые часто имеют левожелудочковую гипертрофию.
Дигиталисный эффект обычно наиболее заметен в отведениях с высокими зубцами R. Помните: дигиталисный эффект - вариант нормы, он ожидаем и не требует прекращения приёма лекарственного средства.
Изменения ЭКГ, связанные с передозировкой (токсичностью) сердечных гликозидов
Токсичные проявления СГ могут потребовать клинического вмешательства. Интоксикация СГ может проявляться блокадами проведения и тахиаритмиями, изолированно или в комбинации.
Супрессия (подавление) синусового узла
Даже при терапевтических дозах СГ синусовый узел можно замедляться, особенно у больных с синдромом слабости синусового узла. При передозировке могут встречаться синоатриальные блокады или полное угнетение синусового узла.
Блокады проведения
СГ замедляют проведение через АВ-узел и могут вызвать АВ-блокады I, II и III степени.
Способность сердечных гликозидов замедлять АВ-проведение используется в лечении наджелудочковой тахикардии. Например, СГ могут замедлять желудочковый ритм у больных с фибрилляцией предсердий; однако, способность СГ замедлять ЧСС хорошо заметна у пациентов в состоянии покоя, но исчезает при физической нагрузке. Бета-блокаторы, такие как атенолол или метопролол, также имеют подобный эффект на АВ-проведение, но могут лучше управлять ЧСС при физической нагрузке или стрессе.
Тахиаритмии
Поскольку СГ увеличивает автоматизм всех клеток проводящей системы, заставляя их действовать как водители ритма, нет тахиаритмии, которую они не могут вызвать. Пароксизмальная предсердная тахикардия и предсердная экстрасистолия являются наиболее распространенными; довольно часты атриовентрикулярные ритмы, трепетание и фибрилляция предсердий.
Комбинации
Комбинация предсердной тахикардии с АВ-блокадой II степени - самое характерное расстройство ритма при интоксикации СГ. Блокада проведения обычно 2:1, но может измениться. Это наиболее распространенная, но не единственная, причина ПТ с блокадой проведения.
Соталол и другие медикаменты, удлиняющие интервал QT
Антиаритмический препарат соталол увеличивает интервал QT и поэтому может, как это ни парадоксально, увеличить риск возникновения желудочковых тахиаритмий. Интервал QT необходимо тщательно проверять у всех пациентов, принимающих соталол. Прием препарата должен быть прекращен при увеличении интервала QT больше, чем на 25%.
Среди других препаратов, которые могут увеличить интервал QT - другие антиаритмические средства (например, хинидин, прокаинамид, дизопирамид, амиодарон и дофетилид), трициклические антидепрессанты, фенотиазины, эритромицин, хинолоновые антибиотики и различные противогрибковые лекарства.
У некоторых пациентов, принимающих хинидин, могут появиться зубцы U. Этот эффект не требует никакого вмешательства.
Несколько наследственных нарушений реполяризации с удлинением интервала QT были идентифицированы и связаны с определенными хромосомными расстройствами. Все люди в этих семьях должны быть проверены на наличие генетического дефекта путем регистрации ЭКГ в состоянии покоя и нагрузки. При обнаружении вышеназванных изменений рекомендуется назначение бета-блокаторов, и иногда имплантируемых дефибрилляторов, поскольку высок риск внезапной смерти. Эти пациенты должны также быть отстранены от спортивных соревнований, им никогда не должны назначаться медпрепараты, которые могут удлинять интервал QT.
Поскольку интервал QT обычно изменяется с частотой сердечных сокращений, используется понятие корректированный интервал QT, или QTc, который используется для оценки абсолютного удлинения QT. QTc приспосабливается к колебаниям частоты сердечных сокращений, определяется путем деления интервала QT на квадратный корень R-R. QTc не должен превысить 500 мс во время терапии любым лекарственным средством, которое может удлинять интервал QT (550 мс, если имеется межжелудочковая блокада); соблюдение этого правила уменьшает риск желудочковых аритмий.
Другие кардиальные нарушения
Перикардит
Острый перикардит может вызвать элевацию сегмента ST и сглаживание зубца T или его инверсию. Эти изменения могут легко быть перепутаны с развивающимся ОИМ. Определенные особенности ЭКГ могут быть полезны в дифференцировании перикардита от инфаркта миокарда:
· Сегмент ST и изменения зубца T при перикардите имеют тенденцию быть диффузными (но не всегда), вовлекая гораздо больше отведений, чем ограниченные изменения при ИМ.
· При перикардите инверсия зубца T обычно встречается только после того, как сегменты ST возвратились к основанию. При инфаркте миокарда инверсия зубца T обычно предшествует нормализации сегментов ST.
· При перикардите формирование зубца Q не наблюдается.
· Иногда снижается интервал PR.
Формирование выпота в полости перикарда уменьшает электрическую мощность сердца, что сопровождается снижением вольтажа во всех отведениях. Изменения сегмента ST и зубца T могут быть незаметны.
Если выпот является достаточно большим, то сердце фактически свободно "плавает" в пределах перикардиальной полости. Это сопровождается феноменом электрических альтернаций, при котором электрическая ось сердца изменяется при каждом сокращении. Может изменяться не только ось комплекса QRS, но также и зубцов P и T. Изменение ЭОС проявляется на ЭКГ изменением амплитуды зубцов от сокращения к сокращению.
Гипертрофическая обструктивная кардиомиопатия (ГОКМ)
Мы уже обсудили гипертрофическую обструктивную кардиомиопатию, прежде известную как идиопатический гипертрофический субаортальный стеноз, в случае пациента Тома Л. Многие пациенты с ГОКМ имеют нормальную ЭКГ, но часто отмечаются левожелудочковая гипертрофия и отклонение электрической оси влево. Иногда могут быть замечены зубцы Q в боковых и нижних отведениях, но они не указывают на ИМ.
Миокардит
Любой диффузный воспалительный процесс, вовлекающий миокард, может вызвать много изменений на ЭКГ. Наиболее распространены блокады проведения, особенно межжелудочковые блокады и гемиблоки.
Заболевания легких
Хроническая обструктивная болезнь легких (ХОБЛ)
ЭКГ пациента с длительной эмфиземой легких может показать низкий вольтаж, отклонение электрической оси вправо и замедленную прогрессию зубца R в грудных отведениях. Низкий вольтаж вызывается эффектом увеличения остаточного объема воздуха в легких. Отклонение электрической оси вправо вызывается расширением легких, смещающих сердце в вертикальное положение.
ХОБЛ может привести к хроническому легочному сердцу и правожелудочковой застойной сердечной недостаточности. ЭКГ в этом случае может показать дилатацию правого предсердия (P-pulmonale) и правожелудочковую гипертрофию с расстройствами реполяризации.
Острая легочная эмболия
Внезапная массивная эмболия легочной артерии может сильно изменить ЭКГ. Результаты исследования могут включать следующее:
· Правожелудочковая гипертрофия с изменениями реполяризации из-за острой правожелудочковой дилатации
· Блокада правой ножки пучка Гиса
(ИМ) остается самой частой причиной вызовов бригад скорой медицинской помощи (СМП). Динамика количества вызовов в г. Москве по поводу ИМ на протяжении трех лет (табл. 1.) отражает стабильность количества вызовов «скорой помощи» по поводу ИМ на протяжении трех лет и постоянство соотношения осложненных и неосложненных инфарктов миокарда. Что касается госпитализаций, то общее их количество практически не изменилось с 1997 до 1999 г. В то же время снизился процент госпитализаций больных с неосложненным ИМ на 6,6% с 1997 к 1999 г.
Таблица 1. Структура вызовов к больным ИМ.
|
Показатель |
1997 |
1998 |
1999 |
|
Количество вызовов к больным ИМ |
|||
|
Неосложненным |
16255 |
16156 |
16172 |
|
Осложненным |
7375 |
7383 |
7318 |
|
Всего |
23630 |
23539 |
23490 |
|
% к общему числу больных сердечно-сосудистыми заболеваниями |
|||
|
Госпитализировано больных |
|||
|
Неосложненным ИМ |
11853 |
12728 |
11855 |
|
Осложненным ИМ |
3516 |
1593 |
3623 |
|
Всего |
15369 |
16321 |
15478 |
|
% госпитализированных больных к количеству вызовов |
|||
|
Неосложненнным ИМ |
79,9 |
78,8 |
73,3 |
|
Осложненным ИМ |
47,6 |
48,7 |
49,5 |
|
Всего |
65,0 |
69,3 |
65,9 |
ОПРЕДЕЛЕНИЕ
Инфаркт миокарда - неотложное клиническое состояние, обусловленное некрозом участка сердечной мышцы в результате нарушения ее кровоснабжения.
ОСНОВНЫЕ ПРИЧИНЫ ВОЗНИКНОВЕНИЯ И ПАТОГЕНЕЗ
Развивающийся в рамках ишемической болезни сердца, является результатом коронарного . Непосредственной причиной инфаркта миокарда чаще всего служит окклюзия или субтотальный стеноз коронарной артерии, почти всегда развивающийся вследствие разрыва или расщепления атеросклеротической бляшки с образованием тромба, повышенной агрегацией тромбоцитов и сегментарным спазмом вблизи бляшки.
КЛАССИФИКАЦИЯ
С точки зрения определения объема необходимой лекарственной терапии и оценки прогноза представляют интерес три классификации.
А. По глубине поражения (на основе данных электрокардиографического исследования):
1. Трансмуральный и крупноочаговый («Q-инфаркт») - с подъемом сегмента ST в
Первые часы заболевания и формированием зубца Q в последующем.
2. Мелкоочаговый («не Q-инфаркт») - не сопровождающийся формированием зубца Q, а
Проявляющийся отрицательными зубцами Т
Б. По клиническому течению:
1. Неосложненный инфаркт миокарда.
2. Осложненный инфаркт миокарда (см. ниже).
В. По локализации:
1. Инфаркт левого желудочка (передний, задний или нижний, перегородочный)
2. Инфаркт правого желудочка.
КЛИНИЧЕСКАЯ КАРТИНА
По симптоматике острейшей фазы инфаркта миокарда выделяют следующие клинические варианты:
|
Болевой (status anginosus) |
- типичное клиническое течение, основным проявлением при котором служит ангинозная боль, не зависящая от позы и положения тела, от движений и дыхания, устойчивая к нитратам; боль имеет давящий, душащий, жгущий или раздирающий характер с локализацией за грудиной, во всей передней грудной стенке с возможной иррадиацией в плечи, шею, руки, спину, эпигастальную область; характерны сочетание с гипергидрозом, резкой общей слабостью, бледностью кожных покровов, возбуждением, двигательным беспокойством. |
|
Абдоминальный (status gastralgicus) |
- проявляется сочетанием эпигастральных болей с диспептическими явлениями - тошнотой, не приносящей облегчения рвотой, икотой, отрыжкой, резким вздутием живота; возможны ирадиация болей в спину, напряжение брюшной стенки и болезненность при пальпации в эпигастрии. |
|
Атипичный болевой |
- при котором болевой синдром имеет атипичный характер по локализации (например, только в зонах иррадиации - горле и нижней челюсти, плечах, руках и т.д.) и/или по характеру. |
|
Астматический (status astmaticus) |
- единственным признаком при котором является приступ одышки, являющийся проявлением острой застойной сердечной недостаточности (сердечная астма или отек легких). |
|
Аритмический |
- при котором нарушения ритма служат единственным клиническим проявлением или преобладают в клинической картине. |
|
Цереброваскулярный |
- в клинической картине которого преобладают признаки нарушения мозгового кровообращения (чаще - динамического): обморок, головокружение, тошнота, рвота; возможна очаговая неврологическая симптоматика. |
|
Малосимптомный (бессимптомный) |
- наиболее сложный для распознавания вариант, нередко диагностируемый ретроспективно по данным ЭКГ. |
ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ
На догоспитальном этапе оказания медицинской помощи диагноз острого инфаркта миокарда ставится на основании наличия соответствующих:
а) клинической картины
б) изменений электрокардиограммы.
А. Клинические критерии.
При болевом варианте инфаркта диагностическим значением обладают:
- интенсивность (в случаях, когда аналогичные боли возникали ранее, при инфаркте они бывают необычно интенсивными),
- продолжительность (необычно длительный приступ, сохраняющийся более 15-20 минут),
- поведение больного (возбуждение, двигательное беспокойство),
- неэффективность сублингвального приема нитратов.
Таблица 2.
Перечень вопросов, обязательных при анализе болевого синдрома в случае подозрения на острый инфаркт миокарда
|
Вопрос |
Примечание |
|
Когда начался приступ? |
Желательно определить как можно точнее. |
|
Сколько времени длится приступ? |
Менее 15, 15-20 или более 20 мин. |
|
Были ли попытки купировать приступ нитроглицерином? |
Был ли хотя бы кратковременный эффект? |
|
Зависит ли боль от позы, положения тела, движений и дыхания? |
При коронарогенном приступе не зависит. |
|
Были ли аналогичные приступы в прошлом? |
Аналогичные приступы, не завершившиеся инфарктом, требуют дифференциальной диагностики с нестабильной стенокардией и не кардиальными причинами. |
|
Возникали ли приступы (боли или удушья) при физической нагрузке (ходьбе), заставляли ли они останавливаться, сколько они длились (в минутах), как реагировали на нитроглицерин? |
Наличие стенокардии напряжения делает весьма вероятным предположение об остром инфаркте миокарда. |
|
Напоминает ли настоящий приступ ощущения, возникавшие при физической нагрузке по локализации или характеру болей? |
По интенсивности и сопровождающим симптомам приступ при инфаркте миокарда обычно более тяжелый, чем при стенокардии напряжения. |
При любом варианте вспомогательное диагностическое значение имеют:
Гипергидроз,
Резкая общая слабость,
Бледность кожных покровов,
Признаки острой сердечной недостаточности.
Отсутствие типичной клинической картины не может служить доказательством отсутствия инфаркта миокарда.
Б. Электрокардиографические критерии - изменения, служащие признаками:
|
Повреждения |
- дугообразный подъем сегмента ST выпуклостью вверх, сливающийся с положительным зубец T или переходящий в отрицательный зубец T (возможна дугообразная депрессия сегмента ST выпуклостью вниз); |
|
Крупноочагового или Трансмурального инфаркта |
- появление патологического зубца Q и уменьшение амплитуды зубца R или исчезновение зубца R и формирование QS; |
|
Мелкоочагового инфаркта |
- появление отрицательного симметричного зубца T; |
|
Примечания: 1. Косвенным признаком инфаркта миокарда, не позволяющим определить фазу и глубину процесса, является остро возникшая блокада ножек пучка Гиса (при наличии соответствующей клиники). 2. Наибольшей достоверностью обладают электрокардиографические данные в динамике, поэтому электрокардиограммы при любой возможности должны сравниваться с предыдущими. |
|
При инфаркте передней стенки подобные изменения выявляются в I и II стандартных отведениях, усиленном отведении от левой руки (aVL) и соответствующих грудных отведениях (V1, 2, 3, 4, 5, 6). При высоком боковом инфаркте миокарда изменения могут регистрироваться только в отведении aVL и для подтверждения диагноза необходимо снять высокие грудные отведения. При инфаркте задней стенки (нижнем, диафрагмальном) эти изменения обнаруживаются во II, III стандартном и усиленном отведении от правой ноги (aVF). При инфаркте миокарда высоких отделов задней стенки левого желудочка (задне-базальном) изменения в стандартных отведениях не регистрируется, диагноз ставится на основании реципрокных изменений - высоких зубцов R и Т в отведениях V 1 -V 2 (таблица 3).
Рис. 1. Острейшая фаза трансмурального переднего инфаркта миокарда.
Таблица 3. Локализация инфаркта миокарда по данным ЭКГ
|
Тип инфаркта по локализации |
Стандартные отведения |
Грудные отведения |
|||||||||
|
III |
|||||||||||
|
Перегородочный |
|||||||||||
|
Пердне-перегородочный |
|||||||||||
|
Передний |
|||||||||||
|
Распростаненный передний |
|||||||||||
|
Передне-боковой |
|||||||||||
|
Боковой |
|||||||||||
|
Высокий боковой |
|||||||||||
|
Задне-боковой |
|||||||||||
|
Задне-диафрагмальный |
|||||||||||
|
Задне-базальный |
|||||||||||
ЛЕЧЕНИЕ ИНФАРКТА МИОКАРДА
Неотложная терапия преследует несколько взаимосвязанных целей:
1. Купирование болевого синдрома.
2. Восстановление коронарного кровотока.
3. Уменьшение работы сердца и потребности миокарда в кислороде.
4. Ограничение размеров инфаркта миокарда.
5. Лечение и профилактика осложнений инфаркта миокарда.
Применяемые для этого лекарственные средства представлены в таблице 3.
Таблица 3.
Основные направления терапии и лекарственные средства, применяемые в острейшей стадии неосложненного инфаркта миокарда
|
Лекарственное средство |
Направления терапии |
|
|
Морфин внутривенно дробно |
Адекватное обезболивание, снижение пред- и постнагрузки, психо-моторного возбуждения, потребности миокарда в кислороде |
2-5 мг внутривенно каждые 5-15 минут до полного устранения болевого синдрома либо до появления побочных эффектов |
|
Стрептокиназа (стрептаза) |
Восстановление коронарного кровотока (тромболизис), купирование болевого синдрома, ограничение размеров инфаркта миокарда, снижение летальности |
1,5 млн. МЕ внутривенно за 60 минут |
|
Гепарин внутривенно струйно (если не проводится тромболизис) |
Предупреждение или ограничение коронарного тромбоза, профилактика тромбоэмболических осложнений, снижение летальности |
10000-15000 МЕ внутривенно струйно |
|
Нитроглицерин или изосорбида динитрат внутривенно капельно |
Купирование болевого синдрома, уменьшение размеров инфаркта миокарда и летальности |
10 мкг/мин. с увеличением скорости на 20 мкг/мин каждые 5 минут под контролем ЧСС и АД |
|
Бета-адреноблокаторы: пропранолол (обзидан) |
Снижение потребности миокарда в кислороде, купирование болевого синдрома, уменьшение размеров некроза, профилактика фибрилляции желудочков и разрыва левого желудочка, повторных инфарктов миокарда, снижение летальности |
1 мг/мин каждые 3-5 минут до общей дозы 10 мг |
|
Ацетилсалици-ловая кислота (аспирин) |
Купирование и профилактика процессов, связанных с агрегацией тромбоцитов; при раннем(!) назначении снижает летальность |
160-325 мг разжевать; |
|
Магния сульфат (кормагнезин) |
Снижение потребности миокарда в кислороде, купирование болевого синдрома, уменьшение размеров некроза, профилактика нарушений сердечного ритма, сердечной недостаточности, снижение летальности |
1000 мг магния (50 мл 10 %, 25 мл 20 % или 20 мл 25 % раствора) внутривенно в течение 30 минут. |
АЛГОРИТМ ОКАЗАНИЯ МЕДИЦИНСКОЙ ПОМОЩИ БОЛЬНЫМ ОСТРЫМ ИНФАРКТОМ МИОКАРДА НА ДОГОСПИТАЛЬНОМ ЭТАПЕ
А. Неосложненный инфаркт миокарда


Б. Неосложненный инфаркт миокарда или инфаркт миокарда, осложненный упорным болевым синдромом


В. Осложненный инфаркт миокарда
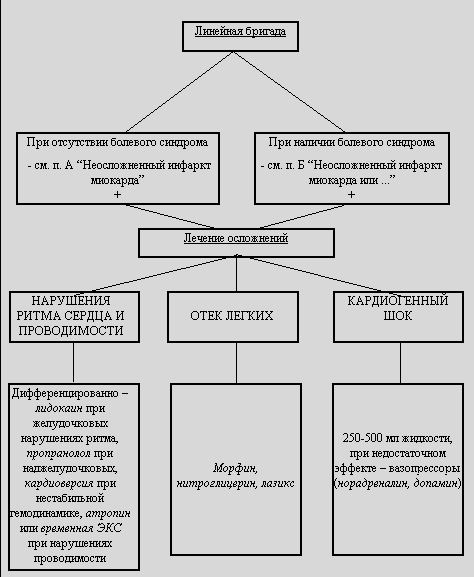
1. Купирование болевого приступа
при остром инфаркте миокарда - одна из важнейших задач, поскольку боль через активацию симпатоадреналовой системы вызывает повышение сосудистого сопротивления, частоты и силы сердечных сокращений, то есть увеличивает гемодинамическую нагрузку на сердце, повышает потребность миокарда в кислороде и усугубляет ишемию.
Если предварительный сублингвальный прием нитроглицерина (повторно по 0,5 мг в таблетках или 0,4 мг в аэрозоле) боль не купировал, начинается терапия наркотическими анальгетиками, обладающими кроме анальгетического и седативного действия влиянием на гемодинамику: вследствие вазодилатирующих свойств они обеспечивают гемодинамическую разгрузку миокарда, уменьшая в первую очередь преднагрузку. На догоспитальном этапе препаратом выбора для купирования болевого синдрома при инфаркте миокарда является морфин, обладающий не только необходимыми эффектами, но и достаточной для транспортировки длительностью действия. Препарат вводится внутривенно дробно: 1 мл 1 % раствора разводят физиологическим раствором натрия хлорида до 20 мл (1 мл полученного раствора содержит 0,5 мг активного вещества) и вводят 2-5 мг каждые 5-15 минут до полного устранения болевого синдрома либо до появления побочных эффектов (гипотензии, угнетения дыхания, рвоты). Суммарная доза не должна превышать 10-15 мг (1-1,5 мл 1% раствора) морфина (на догоспитальном этапе не допускается превышение дозы 20 мг).
При невыраженном болевом синдроме, пациентам старческого возраста и ослабленным больным наркотические анальгетики могут вводиться подкожно или внутримышечно. Не рекомендуется вводить подкожно более 60 мг морфина в течение 12 часов.
Для профилактики и купирования таких побочных эффектов наркотических анальгетиков как тошнота и рвота рекомендуют внутривенное введение 10-20 мг метоклопрамида ( , реглана). При выраженной брадикардии с гипотонией или без нее показано использование атропина в дозе 0,5 мг (0,5 мл 0,1 % раствора) внутривенно; борьба же со снижением артериального давления проводится по общим принципам коррекции гипотензии при инфаркте миокарда.
Недостаточная эффективность обезболивания наркотическими анальгетиками служит показанием к внутривенной инфузии нитратов. При низкой эффективности нитратов в сочетании с тахикардией дополнительный обезболивающий эффект может быть получен введением бета-адреноблокаторов. Боль может быть купирована в результате эффективного тромболизиса.
Упорные интенсивные ангинозные боли служат показанием к применению масочного наркоза закисью азота (обладающей седативным и анальгезирующим действием) в смеси с кислородом. Начинают с ингаляции кислорода в течение 1-3 минут, затем используется закись азота (20 %) с кислородом (80 %) с постепенным повышением концентрации закиси азота до 80 %; после засыпания больного переходят на поддерживающую концентрацию газов - 50 ´ 50 %. Положительный момент - закись азота не влияет на функцию левого желудочка. Возникновение побочных эффектов - тошноты, рвоты, возбуждения или спутанности сознания - является показанием для уменьшения концентрации закиси азота или отмены ингаляции. При выходе из наркоза ингалируют чистый кислород в течение 10 минут для предупреждения артериальной гипоксемии.
Для решения вопроса о возможности использования наркотических анальгетиков следует уточнить ряд моментов:
- убедиться, что типичный или атипичный болевой синдром не является проявлением “острого живота”, и изменения ЭКГ являются специфическим проявлением инфаркта миокарда, а не неспецифической реакцией на катастрофу в брюшной полости;
- выяснить, имеются ли в анамнезе хронические заболевания системы дыхания, в частности, бронхиальная астма;
- уточнить, когда было последнее обострение бронхообструктивного синдрома;
- установить, имеются ли в настоящее время признаки дыхательной недостаточности, какие, какова степень ее выраженности;
- выяснить, имеется ли у больного в анамнезе судорожный синдром, когда был последний припадок.
2. Восстановление коронарного кровотока в острейшей фазе инфаркта миокарда,
достоверно улучшающее прогноз, при отсутствии противопоказаний осуществляется путем системного тромболизиса.
А). Показаниями к проведению тромболизиса служат наличие подъема сегмента ST более чем на 1 mm по крайней мере в двух стандартных отведениях ЭКГ и более чем на 2 mm в двух смежных грудных отведениях или остро возникшая полная блокада левой ножки пучка Гиса при сроке, прошедшем с начала заболевания, более 30 минут, но не превышающем 12 часов. Применение тромболитических средств возможно и позже в случаях когда сохраняются подъем сегмента ST, продолжается боль и/или наблюдается нестабильная гемодинамика.
В отличие от внутрикоронарного системный тромболизис (осуществляется внутривенным введением тромболитических средств) не требует каких-либо сложных манипуляций и специального оборудования. При этом он достаточно эффективен, если начат в первые часы развития инфаркта миокарда (оптимально - на догоспитальном этапе), поскольку сокращение летальности на прямую зависит от сроков его начала.
При отсутствии противопоказаний решение вопроса о проведении тромболизиса основывается на анализе фактора времени: если транспортировка в соответствующий стационар может быть продолжительнее, чем срок до начала этой терапии специализированной бригадой “скорой помощи” (при предполагаемом времени транспортировки более 30 минут или при отсрочке внутрибольничного проведения тромболизиса более чем на 60 минут), введение тромболитических средств должно осуществляться на догоспитальном этапе оказания медицинской помощи. В противном случае оно должно быть отложено до госпитального этапа.
Наиболее часто используется стрептокиназа. Методика внутривенного введения стрептокиназы: введение стрептокиназы проводится только через периферические вены, попытки катетеризации центральных вен недопустимы; перед инфузией возможно внутривенное введение 5-6 мл 25% магния сульфата, либо 10 мл кормагнезина-200 в/в струйно, медленно (за 5 мин); «нагрузочная» доза аспирина (250-300 мг - разжевать) дается всегда, за исключением случаев, когда аспирин противопоказан (аллергические и ); 1 500 000 Ед стрептокиназы разводится в 100 мл изотонического раствора хлорида натрия и вводится внутривенно за 30 мин.
Одновременное назначение гепарина при использовании стрептокиназы не требуется - предполагают, что стрептокиназа сама обладает антикоагуляционными и антиагрегационными свойствами. Показано, что внутривенное введение гепарина не снижает летальность и частоту рецидивов инфаркта миокарда, а эффективность его подкожного введения сомнительна. Если гепарин по каким-либо причинам был введен ранее, это не является препятствием к проведению тромболизиса. Рекомендуется назначение гепарина через 4 ч после прекращения инфузии стрептокиназы. Рекомендовавшееся ранее использование гидрокортизона для профилактики анафилаксии признано не только малоэффективным, но и небезопасным в острейшей стадии инфаркта миокарда (глюкокортикоиды увеличивают риск разрыва миокарда).
Основные осложнения тромболизиса
1). Кровотечения (в т.ч. наиболее грозные - внутричерепные) - развиваются вследствие угнетения процессов свертывания крови и лизиса кровяных сгустков. Риск развития инсульта при системном тромболизисе составляет 0,5-1,5% случаев, обычно инсульт развивается в первые сутки после проведения тромболизиса. Для остановки незначительного кровотечения (из места пункции, изо рта, носа) достаточно сдавления кровоточащего участка. При более значимых кровотечениях (желудочно-кишечном, внутричерепном) необходима внутривенная инфузия аминокапроновой кислоты - 100 мл 5% раствора вводят в течение 30 мин и далее 1 г/час до остановки кровотечения, или транексамовой кислоты по 1-1,5 г 3-4 раза в сутки внутривенно капельно; кроме того эффективно переливание свежезамороженной плазмы. Следует однако помнить о том, что при использовании антифибринолитических средств возрастает риск реокклюзии коронарной артерии и реинфаркта, поэтому использовать их необходимо лишь при угрожающих жизни кровотечениях.
2). Аритмии, возникающие после восстановления коронарного кровообращения (реперфузионные). Не требуют интенсивной терапии медленный узловой или желудочковый ритм (при частоте сердечных сокращений менее 120 в мин и стабильной гемодинамике); наджелудочковая и желудочковая экстрасистолия (в том числе аллоритмированная); атриовентрикулярная блокада I и II (типа Мобитц I) степени. Требуют неотложной терапии фибрилляция желудочков (необходимы дефибрилляция, комплекс стандартных реанимационых мероприятий); двунаправленная веретенообразная желудочковая тахикардия типа «пируэт» (показаны дефибрилляция, введение сульфата магния внутривенно струйно); иные разновидности желудочковой тахикардии (используют введение лидокаина либо проводят кардиоверсию); стойкая суправентрикулярная тахикардия (купируется внутривенным струйным введением верапамила или новокаинамида); атриовентрикулярная блокада II (типа Мобитц II) и III степени, синоатриальная блокада (внутривенно струйно вводят атропин в дозе до 2,5 мг, при необходимости проводят экстренную электрокардиостимуляцию).
3). Аллергические реакции. Сыпь, зуд, периорбитальный отек встречаются в 4,4% случаев, тяжелые реакции ( , анафилактический шок) - в 1,7% случаев. При подозрении на развитие анафилактоидной реакции необходимо немедленно остановить инфузию стрептокиназы и ввести внутривенно болюсом 150 мг преднизолона. При выраженном угнетении гемодинамики и появлении признаков анафилактического шока внутривенно вводят 1 мл 1% раствора адреналина, продолжая введение стероидных гормонов внутривенно капельно. При лихорадке назначают аспирин или парацетамол.
4). Рецидивирование болевого синдрома после проведения тромболизиса купируется внутривенным дробным введением наркотических анальгетиков. При нарастании ишемических изменений на ЭКГ показано внутривенное капельное введение нитроглицерина или, если инфузия уже налажена, - увеличение скорости его введения.
5). При артериальной гипотонии в большинстве случаев бывает достаточно временно прекратить инфузию тромболитика и поднять ноги пациента; при необходимости уровень АД корректируется введением жидкости, вазопрессоров (допамина или норадреналина внутривенно капельно до стабилизации систолического АД на уровне 90-100 мм рт.ст.).

Рис. 2. Реперфузионная аритмия при трансмуральном заднем инфаркте миокарда: эпизод узлового ритма с самостоятельным восстановлением синусового ритма.
Клинические признаки восстановления коронарного кровотока:
- прекращение ангинозных приступов через 30-60 мин после введения тромболитика,
- стабилизация гемодинамики,
- исчезновение признаков левожелудочковой недостаточности,
- быстрая (в течение нескольких часов) динамику ЭКГ с приближением сегмента ST к изолинии и формированием патологического зубца Q, отрицательного зубца Т (возможно внезапное увеличение степени подъема сегмента ST с последующим его быстрым снижением),
- появление реперфузиооных аритмий (ускоренного идиовентрикулярного ритма, желудочковой экстрасистолии и др.),
- быстрая динамику МВ-КФК (резкое повышение ее активности на 20-40%).
Для решения вопроса о возможности использования тромболитичечских средств следует уточнить ряд моментов:
- убедиться в отсутствии в течение предшествовавших 10 дней острых внутренних кровотечений - желудочно-кишечного, легочного, маточного за исключением менструального , гематурии и др. (обратить внимание на их наличие в анамнезе) или хирургических вмешательств и травм с повреждением внутренних органов;
- исключить наличие в течение предшествовавших 2 месяцев острое нарушение мозгового кровообращения, операции или травмы головного или спинного мозга (обратить внимание на их наличие в анамнезе);
- исключить подозрение на острый панкреатит, расслаивающую аневризму аорты, а также на аневризму церебральной артерии, опухоль головного мозга или метастазирующие злокачественные опухоли;
- установить отсутствие физикальных признаков или анамнестических указаний на патологию свертывающей системы крови - геморрагический диатез, тромбоцитопения (обратить внимание на гаморрагическую диабетическую ретинопатию);
- убедиться, что больной не получает непрямые антикоагулянты;
- уточнить, не было ли аллергических реакций на соответствующие тромболитические препараты, а в отношении стрептокиназы, не было ли предшествовавшего ее введения в сроки от 5 дней до 2 лет (в этот период в связи с высоким титром антител введение стрептокиназы недопустимо);
- в случае проведенных успешных реанимационных мероприятий убедиться, что они не были травматичными и длительными (при отсутствии признаков постреанимационных травм - переломов ребер и повреждения внутренних органов обратить внимание на длительность, превышавшую 10 минут);
- добиться стабилизации повышенного артериального давления на уровне менее 200/120 мм рт. ст. (обратить внимание на уровень, превышающий 180/110 мм рт. ст.)
- обратить внимание на другие состояния , опасные развитием геморрагических осложнений и служащие относительными противопоказаниями к проведению системного тромболизиса: тяжелые заболевания печени или почек; подозрение на хроническую аневризму сердца, перикардит, инфекционный миокардит, наличие тромба в сердечных полостях; тромбофлебит и флеботромбоз; варикозное расширение вен пищевода, язвенная болезнь в стадии обострения; беременность;
- иметь в виду, что ряд факторов, не являющиеся относительными или абсолютными противопоказаниями к проведению системного тромболизиса, могут повышать его риск: возраст свыше 65 лет, масса тела менее 70 кг, женский пол, артериальная гипертензия.
Системный тромболизис возможен в пожилом и старческом возрасте, а также на фоне артериальной гипотензии (систолическое АД менее 100 мм рт. ст.) и кардиогенного шока.
В сомнительных случаях решение о проведении тромболитической терапии должно быть отсрочено до стационарного этапа лечения. Отсрочка показана при атипичном развитии заболевания, неспецифических изменениях ЭКГ, давно существующей блокаде ножки пучка Гиса и несомненном предшествующем инфаркте миокарда, маскирующем типичные изменения.
Б). Отсутствие показаний к тромболитической терапии (поздние сроки, так называемый мелкоочаговый или не-Q-инфаркт), невозможность проведения тромболизиса по организационным причинам, а также его отсрочка до госпитального этапа или некоторые противопоказния к нему, не являющиеся противопоказанием к назначению гепарина, служат показанием (при отсутствии собственных противопоказаний) к проведению антикоагулянтной терапии. Ее цель заключается в предупреждении или ограничении тромбоза венечных артерий, а также в профилактике тромбоэмболических осложнений (особенно частых у больных передним инфарктом миокарда, при низком сердечном выбросе, мерцательной аритмии). Для этого на догоспитальном этапе (линейной бригадой) внутривенно болюсно вводится гепарин в дозе 10000-15000 МЕ. Если в условиях стационара не проводится тромболитическая терапия, то переходят на длительную внутривенную инфузию гепарина со скоростью 1000 МЕ/час под контролем активированного частичного тромбопластинового времени. Альтернативой может, по-видимому, служить подкожное введение низкомолекулярного гепарина в "лечебной" дозе. Введение гепарина на догоспитальном этапе не служит препятствием к проведению тромболизиса в условиях стационара.
Несмотря на более высокую безопасность гепаринотерапии по сравнению с системным тромболизисом, в связи со значительно меньшей ее эффективностью ряд противопоказаний к ее проведению имеет значительно более жесткий характер, а некоторые относительные противопоказания к тромболизису оказываются абсолютными для гепаринотерапии. С другой стороны гепарин можно назначать больным с некоторыми противопоказаниями к применению тромболитических средств.
Для решения вопроса о возможности назначения гепарина следует уточнить те же моменты, что и для тромболитичечских средств:
- исключить наличие в анамнезе геморрагического инсульта, операций на головном и спинном мозге;
- убедиться в отсутствии опухоли и язвенной болезни желудка и двенадцатиперстной кишки, инфекционного эндокардита, тяжелого поражения печени и почек;
- исключить подозрение на острый панкреатит, расслаивающую аневризму аорты, острый перикардит с шумом трения перикарда, выслушиваемым в течение нескольких дней(!) (опасность развития гемоперикарда);
- установить отсутствие физикальных признаков или анамнестических указаний на патологию свертывающей системы крови (геморрагические диатезы, болезни крови);
Выяснить, нет ли у больного повышенной чувствительности к гепарину;
- добиться стабилизации повышенного артериального давления на уровне менее 200/120 мм рт. ст.
В). С первых минут инфаркта миокарда всем больным при отсутствии противопоказаний показано назначение малых доз ацетилсалициловой кислоты (аспирина), антитромбоцитарный эффект которой достигает своего максимума уже через 30 минут и своевременное начало применения которой позволяет существенно снизить летальность. Наибольший клинический эффект может быть получен при применении ацетилсалициловой кислоты перед проведением тромболизиса. Доза для первого приема на догоспитальном этапе составляет 160-325 мг, разжевать(!). В дальнейшем, на стационарном этапе, препарат назначается 1 раз в сутки по 100-125 мг.
Для решения вопроса о возможности назначения ацетилсалициловой кислоты имеет значение лишь небольшая часть ограничений для тромболитичечских средств; необходимо уточнить:
Имеются ли у больного эрозивно-язвенные поражения ЖКТ в стадии обострения;
Имелись ли в анамнезе желудочно-кишечные кровотечения;
Нет ли у больного анемии;
- нет ли у больного “аспириновой триады” ( , полипоз носа,
Непереносимость аспирина);
Имеется ли повышенная чувствительность к препарату?
3. Уменьшение работы сердца и потребности миокарда в кислороде
кроме полноценного обезболивания обеспечивается применением
а) вазодилататоров - нитратов,
б) бета-адреноблокаторов и
в) средствами комплексного воздействия - магния сульфата.
А. Внутривенное введение нитратов при остром инфаркте миокарда не только помогает купировать болевой синдром, левожелудочковую недостаточность, артериальную гипертензию, но и уменьшает размеры некроза и летальность. Растворы нитратов для внутривенного введения готовят ex tempore: каждые 10 мг нитроглицерина (например, 10 мл 0,1 % раствора в виде препарата перлинганит) или изосорбида динитрата (например, 10 мл 0,1 % раствора в виде препарата изокет) разводят в 100 мл физиологического раствора (20 мг препарата - в 200 мл физиологического раствора и т.д.); таким образом 1 мл приготовленного раствора содержит 100 мкг, а 1 капля - 5 мкг препарата. Нитраты вводят капельно под постоянным контролем артериального давления и частоты сердечных сокращений с начальной скоростью 5-10 мкг/мин с последующим увеличением скорости на 20 мкг/мин каждые 5 минут до достижения желаемого эффекта или максимальной скорости введения - 400 мкг/мин. Обычно эффект достигается при скорости 50-100 мкг/мин. При отсутствии дозатора приготовленный раствор, содержащий в 1 мл 100 мкг нитрата, вводят при тщательном контроле (см. выше) с начальной скоростью 6-8 капель в минуту, которая при условии стабильной гемодинамики и сохранения болевого синдрома может быть постепенно увеличена вплоть до максимальной скорости - 30 капель в минуту. Введение нитратов проводится как линейными, так и специализированными бригадами и продолжается в стационаре. Продолжительность внутривенного введения нитратов - 24 часа и более; за 2-3 часа до окончания инфузии дается первая доза нитратов перорально. Передозировка нитратов, вызывающая падение сердечного выброса и снижение систолического артериального давления ниже 80 мм рт. ст., может приводить к ухудшению коронарной перфузии и к увеличению размеров инфаркта миокарда.
Для решения вопроса о возможности назначения нитратов необходимо уточнить ряд моментов:
- убедиться, что систолическое артериальное давление выше 90 мм рт. ст. (для короткодействующего нитроглицерина) или выше 100 мм рт. ст (для более продолжительно действующего изосорбида динитрата);
- исключить наличие стеноза устья аорты и гипертрофической кардиомиопатии с обструкцией выносного тракта (аускультативно и по данным ЭКГ), тампонаду сердца (клиническая картина венозного застоя по большому кругу кровообращения при минимальных признаках левожелудочковой недостаточности) и констриктивный перикардит (триада Бека: высокое венозное давление, асцит, “малое тихое сердце”);
- исключить внутричерепную гипертензию и острую церебральную дисциркуляцию (в том числе как проявления инсульта, острой гипертонической энцефалопатии, недавно перенесенной черепно-мозговой травмы);
- исключить возможность провокации нитратами развития синдрома малого выброса вследствие поражения правого желудочка при инфаркте или ишемии правого желудочка, которые могут сопутствовать задней (нижней) локализации инфаркта левого желудочка, или при тромбоэмболии легочной артерии с формированием острого легочного сердца;
- убедиться с помощью пальпаторного обследования в отсутствии высокого внутриглазного давления (при закрытоугольной глаукоме);
- уточнить, нет ли у больного непереносимости нитратов.
Б. Внутривенное введение бета-адреноблокаторов
также как и применение нитратов способствует купированию болевого синдрома; ослабляя симпатические влияния на сердце (эти влияния усилены в первые 48 часов инфаркта миокарда вследствие самого заболевания и в результате реакции на боль) и снижая потребность миокарда в кислороде, они способствуют уменьшению размеров инфаркта миокарда, подавляют желудочковые аритмии, уменьшают риск разрыва миокарда и повышают таким образом выживаемость пациентов. Очень важно, что бета-адреноблокаторы согласно экспериментальным данным позволяют отсрочить гибель ишемизированных кардиомиоцитов (они увеличивают время, в течение которого окажется эффективным тромболизис).
При отсутствии противопоказаний бета-адреноблокаторы назначаются всем больным острым инфарктом миокарда. На догоспитальном этапе показаниями к их внутривенному введению служат для линейной бригады - соответствующие нарушения ритма, а для специализированной - упорный болевой синдром, тахикардия, артериальная гипертензия. В первые 2-4 часа заболевания показано дробное внутривенное введение пропранолола (обзидана) по 1 мг в минуту каждые 3-5 минут под контролем артериального давления, частоты сердечных сокращений и ЭКГ до достижения частоты сердечных сокращений 55-60 уд./мин или до общей дозы 10 мг. При наличии брадикардии, признаков сердечной недостаточности, AV-блокакды и снижении систолического артериального давления менее 100 мм рт. ст. пропранолол не назначается, а при развитии указанных изменений на фоне его применения введение препарата прекращается.
Для решения вопроса о возможности назначения бета-адреноблокаторов необходимо уточнить ряд моментов:
- убедиться в отсутствии острой сердечной недостаточности или недостаточности кровообращения II-III стадии, артериальной гипотензии;
- исключить наличие AV блокады, синоатриальной блокады, синдрома слабости синусового узла, брадикардии (ЧСС менее 55 ударов в минуту);
- исключить наличие бронхиальной астмы и других обструктивных заболеваний дыхательных путей, а также вазомоторного ринита;
- исключить наличие облитерирующих заболеваний сосудов ( или эндартерит, синдром Рейно и др.);
В) Внутривенная инфузия магния сульфата
проводится у больных с доказанной или вероятной гипомагнезиемией или при синдроме удлиненного QT, а также в случае осложнения инфаркта миокарда некоторыми вариантами аритмий. При отсутствии противопоказаний магния сульфат может служить определенной альтернативой применению нитратов и бета-адреноблокаторов, если их введение по какой-то причине невозможно (противопоказания или отсутствие). По результатам ряда исследований он, как и другие средства, уменьшающие работу сердца и потребность миокарда в кислороде, снижает летальность при остром инфаркте миокарда, а также предотвращает развитие фатальных аритмий (в том числе, реперфузионных при проведении системного тромболизиса) и постинфарктной сердечной недостаточности. При лечении острого инфаркта миокарда 1000 мг магния (50 мл 10 %, 25 мл 20 % или 20 мл 25 % раствора сернокислой магнезии) вводятся внутривенно капельно в течение 30 минут в 100 мл изотонического раствора натрия хлорида; в последующем проводится внутривенная капельная инфузия в течение суток со скоростью 100-120 мг магния в час (5-6 мл 10 %, 2,5-3 мл 20 % или 2-2,4 мл 25 % раствора сернокислой магнезии).
Для решения вопроса о показаниях к назначению магния сульфата необходимо уточнить ряд моментов:
- выявить клинические и анамнестические признаки возможной гипомагнезиемии - гиперальдостеронизм (в первую очередь при застойной сердечной недостаточности и стабильной атрериальной гипертензии), гипертиреоз (в том числе ятрогенный), хроническая алкогольная интоксикация, судорожные сокращения мышц, длительное применение диуретиков, глюкокортикоидная терапия;
- диагностировать наличие синдрома удлиненного QT по ЭКГ.
Для решения вопроса о возможности назначения магния сульфата необходимо уточнить ряд моментов:
- убедиться в отсутствии состояний, проявляющихся гипермагнезиемией - почечной недостаточности, диабетического кетоацидоза, гипотиреоза;
- исключить наличие AV блокады, синоаурикулярной блокады, синдрома слабости синусового узла, брадикардии (ЧСС менее 55 ударов в минуту);
Исключить наличие у больного миастении;
- уточнить, нет ли у больного непереносимости препарата.
4. Ограничение размеров инфаркта миокарда
достигается адекватным обезболиванием, восстановлением коронарного кровотока и уменьшением работы сердца и потребности миокарда в кислороде.
Этой же цели служит оксигенотерапия, показанная при остром инфаркте миокарда всем больным в связи с частым развитием гипоксемии даже при неосложненном течении заболевания. Ингаляция увлажненного кислорода, проводящаяся, если это не причиняет чрезмерных неудобств, с помощью маски или через носовой катетер со скоростью 4-6 л/мин, целесообразна в течение первых 24-48 часов заболевания (начинается на догоспитальном этапе и продолжается в стационаре).
5. Лечение и профилактика осложнений инфаркта миокарда.
Все перечисленные мероприятия вместе с обеспечением физического и психического покоя, госпитализацией на носилках служат профилактике осложнений острого инфаркта миокарда. Лечение же в случае их развития проводится дифференцированно в зависимости от варианта осложнений: отек легких, кардиогеннй шок, нарушения сердечного ритма и проводимости, а также затянувшийся или рецидивирующий болевой приступ.
1). При острой левожелудочковой недостаточности с развитием сердечной астмы или отека легких одновременно с введением наркотических анальгетиков и нитроглицерина внутривенно струйно вводят 40-120 мг (4-12 мл) раствора фуросемида (лазикса), максимальная доза на догоспитальном этапе - 200 мг.
2). Основой лечения кардиогенного шока служит ограничение зоны повреждения и увеличение объёма функционирующего миокарда путём улучшения кровоснабжения его ишемизированных участков, для чего проводится системный тромболизис.
Аритмический шок требует немедленного восстановления адекватного ритма путем проведения электроимпульсной терапии, электрокардиостимуляция, при невозможности их проведения показана медикаментозная терапия (см. далее).
Рефлекторный шок купируется после проведения адекватной анальгезии; при исходной брадикардии опиоидные анальгетики нужно сочетать с атропином в дозе 0,5 мг.
Истинный кардиогенный шок (гипокинетический тип гемодинамики ) служит показанием к в/в капельному введению негликозидных кардиотонических (положительных инотропных) средств - допамина, добутамина, норэпинефрина. Этому должна предшествовать коррекция гиповолемии. При отсутствии признаков застойной левожелудочковой недостаточности ОЦК корригируется струйным введением 0,9% раствора натрия хлорида в объёме до 200 мл за 10 мин с повторным введением той же дозы при отсутствии эффекта или осложнений.
Допамин в дозе 1-5 мкг/кг/мин оказывает преимущественно вазодилатирующее действие, 5-15 мкг/кг/мин - вазодилатирующее и положительное инотропное (и хронотропное) действие, 15-25 мкг/кг/мин - положительное инотропное (и хронотропное) и периферическое вазоконстриктивное действие. Начальная доза составляет 2-5 мкг/кг/мин с постепенным увеличением до оптимальной.
Добутамин в отличие от допамина не вызывает вазодилатацию, но обладает мощным положительным инотропным эффектом и менее выраженными увеличением ЧСС и аритмогенном эффектом. Препарат назначается в дозе 2,5 мкг/кг/мин с увеличением каждые 15-30 мин на 2,5 мкг/кг/мин до получения эффекта, побочного действия или достижения дозы 15 мкг/кг/мин.
Комбинация допамина с добутамином в максимально переносимых дозах используется при отсутствии эффекта от максимальной дозы одного из них или при невозможности использования максимальной дозы одного препарата из-за появления побочных эффектов (синусовая тахикардия более 140 в минуту или желудочковая аритмия).
Комбинация допамина или добутамина с норэпинефрином, назначаемым в дозе 8 мкг/мин.
Норэпинефрин (норадреналин) в качестве монотерапии применяется при невозможности использовать другие прессорные амины. Назначается в дозе, не превышающей 16 мкг/мин, в обязательном сочетании с инфузией нитроглицерина или изосорбида динитрата со скоростью 5-200 мкг/мин.
3). Желудочковая экстрасистолия в острой стадии инфаркта миокарда может быть предвестником фибрилляции желудочков. Препарат выбора для лечения желудочковых нарушений ритма - лидокаин - вводится внутривенно болюсом из расчета 1 мг/кг массы с последующей капельной инфузией 2-4 мг/мин. Не рекомендуется применявшееся ранее профилактическое назначение лидокаина всем больным острым инфарктом миокарда (препарат увеличивает летальность вследствие асистолии). Больным с застойной сердечной недостаточностью, заболеваниями печени, вводят в дозе, сниженной вдвое.
При желудочковой тахикардии, трепетании предсердий и мерцательной аритмии с высокой ЧСС и нестабильной гемодинамикой средством выбора является дефибрилляция. При мерцательной тахиаритмии и стабильной гемодинамике используют (анаприлин, обзидан) для урежения ЧСС.
При развитии атрио-вентрикулярной блокады II-III степени внутривенно вводят 1 мл 0,1% раствора атропина, при неэффективности пробной терапии атропином и появлении обмороков (приступов Морганьи-Эдемса-Стокса) показана временная электрокардиостимуляция.
ЧАСТО ВСТРЕЧАЮЩИЕСЯ ОШИБКИ ТЕРАПИИ.
Высокая летальность в первые часы и сутки инфаркта миокарда обусловливает необходимость назначения адекватной медикаментозной терапии, начиная с первых минут заболевания. Потеря времени значительно ухудшает прогноз.
А. Ошибки, обусловленные устаревшими рекомендациями, частично сохраняющимися и в некоторых современных стандартах оказания медицинской помощи на догоспитальном этапе.
Наиболее распространенной ошибкой является использование трехступенчатой схемы обезболивания: при отсутствии эффекта от сублингвального приема нитроглицерина переход к наркотическим анальгетикам осуществляется только после безуспешной попытки купировать болевой синдром с помощью комбинации ненаркотического анальгетика (метамизола натрия - анальгина) с антигистаминным препаратом (дифенидрамином - димедролом). Между тем, потеря времени при использовании такой комбинации, которая, во-первых, как правило не позволяет получить полной анальгезии, а во-вторых, не способна в отличие от наркотических анальгетиков обеспечить гемодинамическую разгрузку сердца (главную цель обезболивания) и уменьшить потребность миокарда в кислороде, приводит к усугублению состояния и ухудшению прогноза.
Значительно реже, но все еще применяются миотропные спазмолитики (как исключение используется рекомендовавшийся ранее папаверин, на смену которому пришел дротаверин - но-шпа), не улучшающие перфузию пораженной зоны, но повышающие потребность миокарда в кислороде.
Нецелесообразно применение атропина для профилактики (это не касается купирования) вагомиметических эффектов морфина (тошнота, рвота, влияние на сердечный ритм и артериальное давление), поскольку он может способствовать увеличению работы сердца.
Рекомендующееся профилактическое назначение лидокаина всем больным острым инфарктом миокарда без учета реальной ситуации, предупреждая развитие фибрилляции желудочков, может значительно увеличивать летальность вследствие наступления асистолии.
Б. Ошибки, обусловленные другими причинами.
Весьма часто в целях обезболивания при ангинозном статусе неоправданно используется комбинированный препарат метамизол натрия с фенпиверином бромидом и питофеноном гидрохлоридом (баралгин, спазмалгин, спазган и т. д.) или трамадол (трамал), практически не влияющие на работу сердца и потребление кислорода миокардом, а потому не показанные в этом случае (см. выше).
Крайне опасно при инфаркте миокарда применение в качестве антиагрегантного средства и “коронаролитика” дипирадамола (курантила), значительно повышающего потребность миокарда в кислороде.
Весьма распространенной ошибкой является назначение калия и магния аспартата (аспаркама, панангина), не влияющего ни на внешнюю работу сердца, ни на потребление миокардом кислорода, ни на коронарный кровоток и т.д.
ПОКАЗАНИЯ К ГОСПИТАЛИЗАЦИИ.
Острый инфаркт миокарда является прямым показанием к госпитализации в отделение (блок) интенсивной терапии или кардиореанимации. Транспортировка осуществляется на носилках.
